疾病負擔與流行病學
Secondary mitral regurgitation (SMR) 是心臟衰竭患者最常見的瓣膜病變。根據 European Society of Cardiology Heart Failure Long-Term Registry 資料,中度至重度 SMR 在 HFrEF 患者中盛行率達 36%,HFmrEF 為 28%,HFpEF 為 20%[1]。在急性失代償性心衰患者中,LVEF <50% 者 moderate-severe MR 盛行率更高達 44.5%[2]。
SMR 的預後影響深遠。社區世代研究顯示,重度 SMR 患者死亡率較同齡同性別人群高出 7.5 倍(HR 7.53, 95% CI 6.83–8.30)[3]。獨立於臨床及超音波混雜因子,重度 SMR 使死亡率增加 76%。重要的是,SMR 的負擔預計將隨人口老化持續增加。
SMR 不僅是心衰的「結果」,更是心衰惡化的「驅動因素」。Volume overload → LV dilation → annular dilation → 更多 MR → 更多 volume overload,形成惡性循環。打斷這個循環是治療的核心理據。
病理生理學:為什麼 SMR 有不同表型?
SMR 的機轉是多因素的。二尖瓣裝置(annulus、leaflets、chordae、papillary muscles)與左心室高度相互依存。MV 並非被動結構;其 annulus 具有主動的 sphincteric 特性,與心室收縮功能密切相關[4]。
SMR 可根據病因分為兩大表型:
| 表型 | 機轉 | LVEF | LV/LA 特徵 | 治療考量 |
|---|---|---|---|---|
| Ventricular SMR (V-SMR) | LV remodeling → papillary muscle displacement → leaflet tethering | <50% | LV 擴大,± LA 擴大 | GDMT + CRT + TEER |
| — Proportionate | MR 嚴重度與 LV 擴大「成比例」 | <40% | 嚴重 LV 擴大 (LVEDV >250 mL) | GDMT 為主;TEER 效果有限(MITRA-FR) |
| — Disproportionate | MR 嚴重度「超過」LV 擴大預期 | 20–50% | 輕中度 LV 擴大 (LVEDV <200 mL) | TEER 獲益最大(COAPT) |
| Atrial SMR (A-SMR) | LA dilation → annular dilation → leaflet malcoaptation | ≥50% | LA 嚴重擴大,LV 正常 | AF management + ? TEER (IIb) |
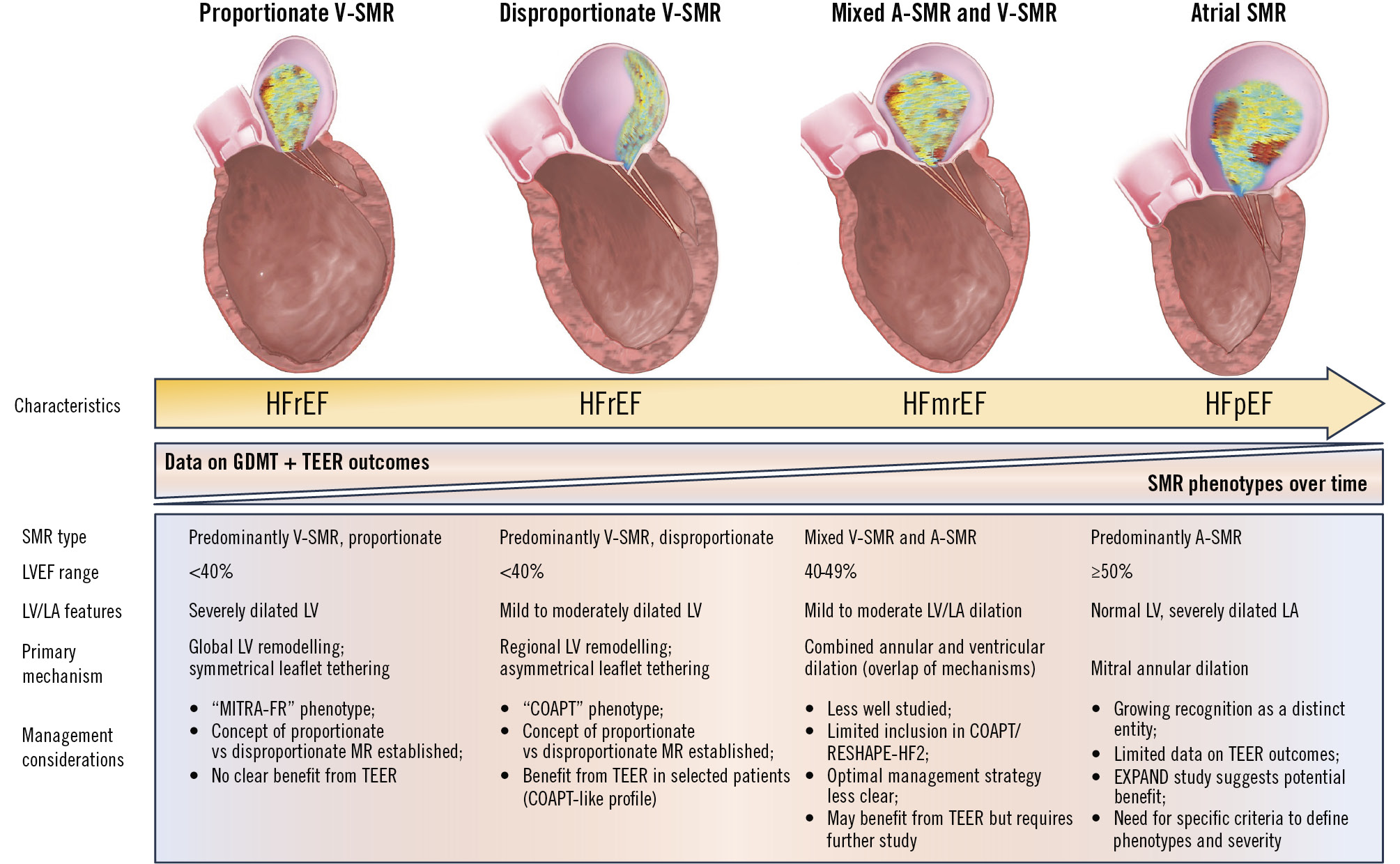
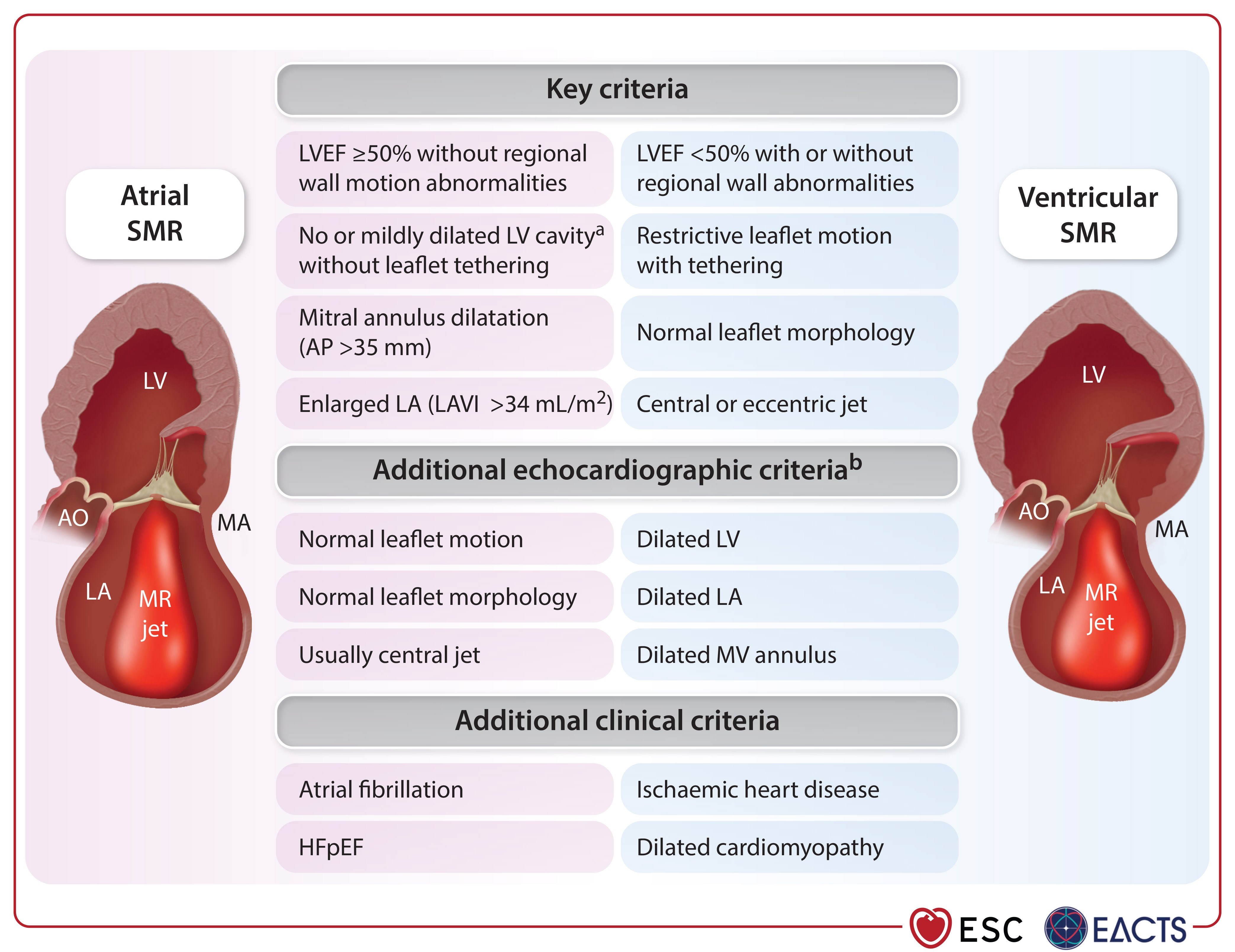
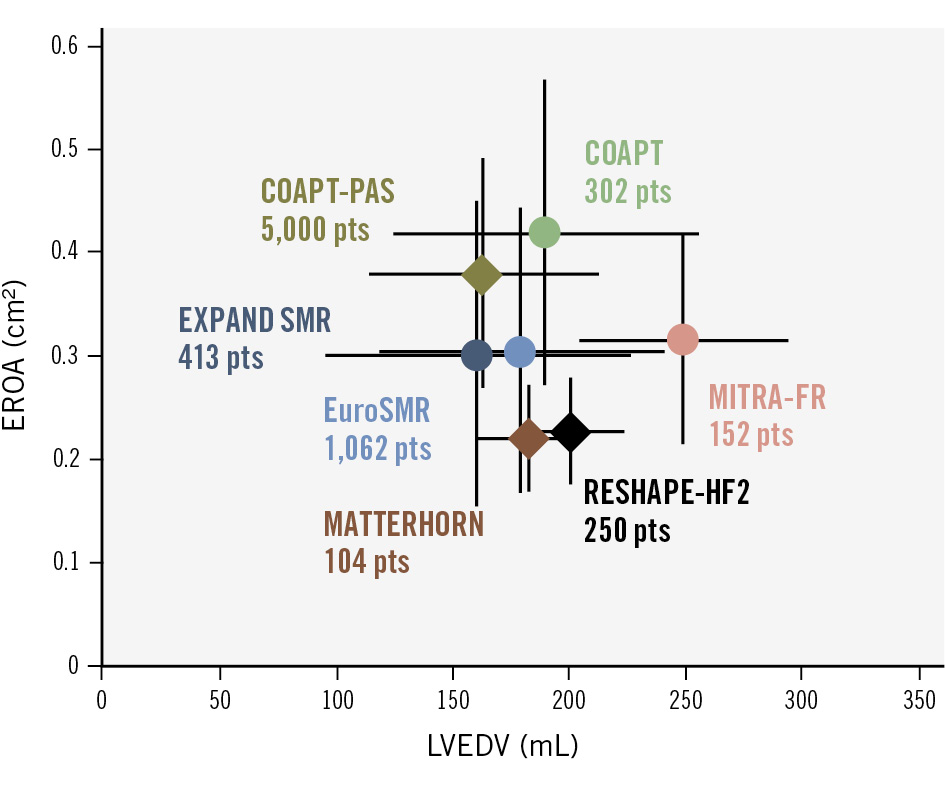
Grayburn 等人提出的框架[5]用 EROA/LVEDV 比值來區分:COAPT 患者(mean EROA 0.40 cm², LVEDV 193 mL)為典型 disproportionate MR;MITRA-FR 患者(EROA 0.31 cm², LVEDV ~260 mL)為 proportionate MR。然而,EuroIntervention 2025 SOTA 指出此框架「從未被證實能在臨床上有效區分 TEER 獲益者」[4],因 SMR 具有動態性,固定時間點的分類可能不夠精確。
Unmet Needs:為什麼光靠藥物不夠?
儘管 GDMT(包括 ACEi/ARB/ARNI、beta-blockers、MRA、SGLT2i 四柱治療)是 HFrEF 管理的基石,近 60% 的 SMR 患者在 GDMT 優化後仍有顯著 SMR 改善[4]。然而,這也意味著 ~40% 的患者即使在最佳藥物治療後,SMR 仍持續存在,繼續承受高住院率和死亡風險。
Sacubitril/valsartan 可使 EROA 降低約 34.6%,約 50% 的重度 SMR 患者可改善至非重度[4]。SGLT2i 也顯示可減少 functional MR。但這些新藥在三大 RCT(COAPT 2018, MITRA-FR 2018, RESHAPE-HF2 2024)進行時尚未被廣泛使用,因此「四柱 GDMT + TEER」的組合效果仍是未解之問[6]。
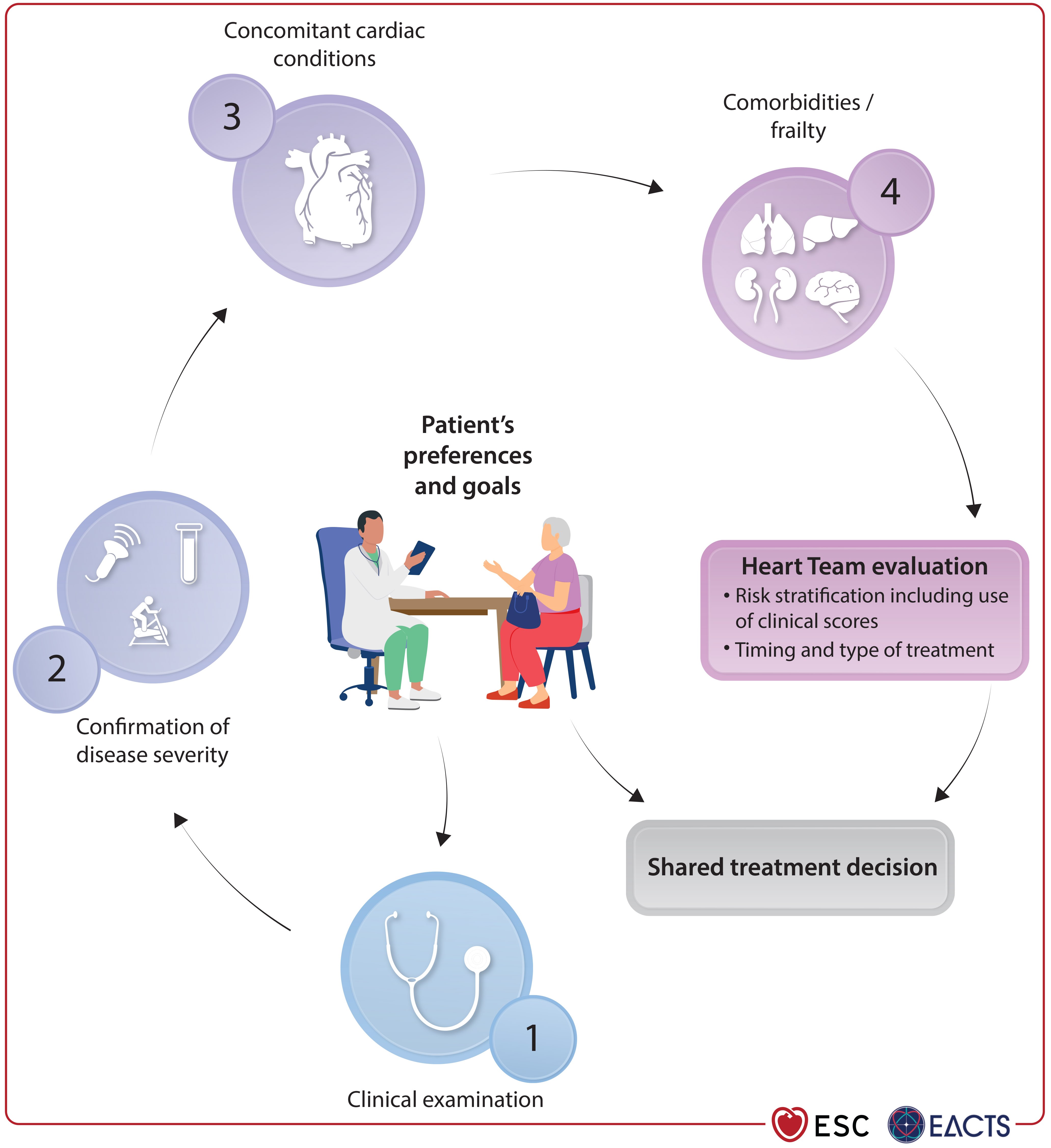
三大 Landmark RCTs 的啟示
| 特徵 | COAPT (2018) | MITRA-FR (2018) | RESHAPE-HF2 (2024) |
|---|---|---|---|
| 人數 | 614 | 307 | 505 |
| MR 嚴重度 | 3+ 至 4+(mean EROA 0.40 cm²) | Severe(mean EROA 0.31 cm²) | 3+ 至 4+(median EROA 0.23 cm²) |
| Mean LVEDV | 193 mL | ~260 mL | median 200 mL(介於兩者之間) |
| Mean LVEF | 31% | 33% | 31–32%(median) |
| HF 住院 | HR 0.53 (0.40–0.70) ✓ | HR 0.97 (0.72–1.30) ✗ | RR 0.59 (0.42–0.82) ✓ |
| 全因死亡 | HR 0.62 (0.46–0.82) ✓ | HR 1.02 (0.70–1.50) ✗ | HR 0.73 (0.51–1.05) — |
| HFH + CV death | 顯著降低 | 無差異 | RR 0.64 (0.48–0.85) ✓ |
| KCCQ 改善 | 顯著改善 | 無差異 | +10.9 points (6.8–15.0) ✓ |
| 5 年追蹤 | 獲益持續至 5 年 | 延遲分析:12–24 月 HFH HR 0.46 | 尚待長期追蹤 |
| MR 表型 | Disproportionate | Proportionate | 介於兩者之間 |
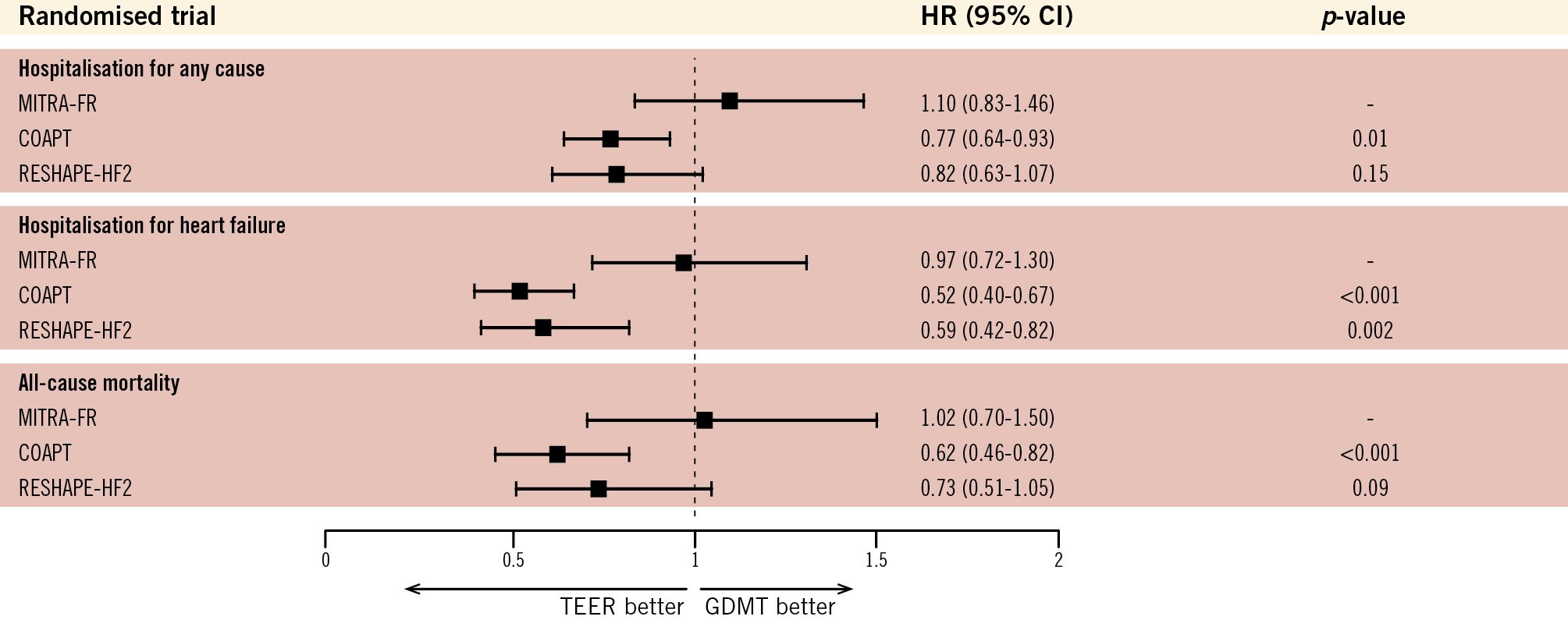
三大 RCTs 收案標準比較
| 收案條件 | COAPT (2018) | MITRA-FR (2018) | RESHAPE-HF2 (2024) |
|---|---|---|---|
| MR 嚴重度 | Grade 3+ 或 4+ Independent echo core lab 確認 (3-tier multiparametric algorithm;Iung Circulation 2020) |
Severe secondary MR(Carpentier Type IIIb restrictive):EROA >20 mm² 或 RVol >30 mL CoreLab(Hôpital Bichat)隨機化前確認所有 echo criteria |
Moderate-severe 或 severe functional MR Echo core lab 確認 (依 EAE 標準;core lab 確認 MR severity) |
| LVEF 範圍 | 20–50% | 15–40% | 20–50% (初始:NYHA II 15–35%;NYHA III–IV 15–45%;後修訂) |
| LVESD 上限 | ≤70 mm | 未規定 | 未規定 |
| NYHA Class | II, III, IVa(ambulatory) | ≥ II(含 IV) | II, III, IV |
| GDMT 要求 | Stable maximal tolerated doses of GDMT + CRT(if appropriate) 由 CEC 審查 GDMT 優化程度 |
Traitement médical optimisé 由 investigator 判定,包含 ACEi/ARB、BB、MRA(依 ESC guidelines) |
ESC/HFA guideline-recommended therapy;randomisation 前 2 週內不可有新 HF drug class 或 dose change(diuretics 除外) 須先完成 revasc + CRT(if eligible)≥90 天 |
| HF 住院 / BNP 門檻 | ≥1 次 HF 住院(12 月內)或 corrected BNP ≥300 或 NT-proBNP ≥1500 pg/mL (BNP 經 BMI 校正:BMI >20 時每增 1 kg/m² 切點降 4%) |
≥1 次 HF 住院(12 月內)— 必要條件 (無 BNP 替代選項) |
HF 住院(12 月內)或 BNP ≥300 / NT-proBNP ≥1000 pg/mL (須於 optimal therapy 穩定後 90 天內取得) |
| 年齡 | ≥18 歲 | >18 歲 | 18–90 歲(設有上限) |
| Central Eligibility Committee | 有 — 獨立委員會逐案審查 GDMT、解剖、手術風險 (篩掉 ~34% 患者) |
無 | 無(local Heart Team 決定) |
| Echo Core Lab 角色 | 確認 MR severity(3-tier algorithm) | 隨機化前確認:LVEF 15–40%、EROA >20 mm²/RVol >30 mL、排除 primary MR (每週 teleconference 審查) |
確認 MR severity 及 MVA |
| 心臟手術適合性 | Heart Team 判定 MV surgery not appropriate | Heart Team 判定 not eligible for surgery (至少含 CT surgeon + interventional cardiologist + echocardiographer + anaesthesiologist) |
Heart Team 判定 MV surgery not appropriate |
| 解剖適合性 | Non-commissural primary jet treatable by MitraClip;CEC + echo core lab 三層審查 | Site PI 評估 + Abbott proctor 確認 procedural feasibility (CoreLab 排除 primary MR、確認 LVEF/EROA/RVol) |
Site investigator 評估 leaflet anatomy + echo core lab 確認 MVA 排除 IVC filter 干擾 delivery catheter;排除 TEE contraindication;排除 transseptal catheterization contraindication |
| Vascular access | 明確要求:transseptal catheterisation + femoral vein access 須 feasible | 未明確列出 | 未明確列出 |
| 其他特殊要求 | CK-MB < ULN(14 天內) | 法國 Sécurité Sociale 加入;排除 uncontrolled HTN(三階分級:非糖尿病 >140/90、糖尿病/CKD >130/90、>80 歲 >150 SBP);排除 nitinol 過敏;排除嚴重肝功能不全(Factor V <50%) | 須能行走 + 完成 6MWT(≤475 m) NYHA IV 豁免 6MWT;LVEF 須 TTE/contrast ventriculography/gated scan/MRI 確認(90 天內) |
| 收案地區 / 中心數 | 78 centers,美國+加拿大 | 37 centers,法國 | 51 centers,歐洲 8 國 |
實際收錄病人基線特徵(Baseline Characteristics)
| 特徵 | COAPT (N=614) | MITRA-FR (N=304) | RESHAPE-HF2 (N=505) |
|---|---|---|---|
| 年齡 | 72.2 ± 11.2 yr | 70.4 ± 10.0 yr | 69.7 ± 10.6 yr |
| 男性 | 64.0% | 74.7% | 80.4% |
| Ischemic CM | 60.7% | 59.2% | 65.1% |
| NYHA II / III / IV | 32.0% / 53.4% / 14.6% | 32.9% / 58.6% / 8.6% | 24.6% / 60.0% / 15.2% |
| Diabetes | 37.3% | 29.3% | 34.9% |
| AF history | 55.2% | 33.6% | 48.1% |
| Previous CRT | 36.5% | 32.2% (CRT-D or CRT-P, main text Table 1) |
30.9% (device) / 26.7% (control) |
| Previous ICD | — | — | 30.1% (device) / 40.4% (control) |
| STS score / EuroSCORE II | STS 8.2 ± 5.9% | EuroSCORE II median 6.3 | EuroSCORE II median 5.3 (IQR 2.8–9.0) |
| LVEF | 31.3 ± 9.3% | 33.1 ± 6.6% | median 31% (device) / 32% (control) |
| LVEDV | 193 ± 71 mL | 135 ± 35 mL/m² (indexed;~260 mL estimated unindexed) |
median 200 mL (IQR 153–249) |
| LVESV | 135 ± 58 mL | — | median 137 mL (IQR 100–173) (core lab; Appendix Table S5) |
| LVEDd / LVESd | — | — | LVEDd 6.9 (6.3–7.6) / LVESd 5.8 (5.3–6.5) cm (core lab; Appendix Table S5) |
| MR Grade 3+ / 4+ | 52.2% / 47.8% | —(以 EROA/RVol 定義) | 55.8% / 44.2% |
| EROA | 0.41 ± 0.15 cm² (core lab 確認) |
0.31 ± 0.10 cm² | median 0.23 cm² (IQR 0.20–0.30) |
| RVol | — | 45 ± 13 mL | median 35.5 mL (IQR 28.6–43.2) |
| NT-proBNP | 5559 ± 7502 pg/mL | median 3350 ng/L | median 2734 pg/mL |
| eGFR / CrCl | CrCl 49.4 ± 26.8 mL/min | GFR 49.5 ± 19.9 mL/min | — |
| HF 住院史(1 年內) | — | 100%(必要收案條件) | 65.9% |
| 6MWD | — | — | median 300 m (IQR 218–368) |
| GDMT 使用率 | ACEi/ARB 73% / BB 91% / MRA 56% / diuretics 96% (CEC-adjudicated maximal tolerated dose) |
ACEi/ARB 75% / BB 87% / MRA 60% (protocol 要求 traitement médical optimisé) |
BB 96% / ACEi-ARB-ARNI 82% / MRA 82% / SGLT2i 9% |
解剖收案條件(Anatomical Eligibility)
| 解剖條件 | COAPT | MITRA-FR | RESHAPE-HF2 |
|---|---|---|---|
| MR 病因確認 | Functional MR only:須有 global/regional LVWMA 為 MR 主因 排除 flail leaflet 或任何 degenerative MR 輕度 focal thickening(與老化相關)不排除 FMR |
Secondary MR(依 ESC 定義) CoreLab 隨機化前排除 primary MR 排除 chordal fusion/thickening、commissural fusion、leaflet prolapse/flail |
Functional MR(TEE 確認非 degenerative) |
| MVA 下限 | ≥ 4.0 cm² | 未規定 | ≥ 3.0 cm² (若 MVA 3.0–4.0 cm²:BSA <2.0 m² 且 mean gradient ≤3 mmHg 方可入組) |
| Jet 位置 | Non-commissural primary jet,且 implanting investigator 判斷可由 MitraClip 治療 若有 secondary jet,須為 clinically insignificant |
未明確規定 | 未明確規定 |
| 🔑 MitraClip 解剖適合度 — Leaflet Anatomy Criteria | |||
| Coaptation length (對合長度) |
若有 leaflet tethering:coaptation length 須 ≥ 2 mm 定義:mid-systole 時 leaflet 在 atrial-to-ventricular 方向的接觸長度(或可用長度),於 four-chamber view 測量(見 Protocol Figure 4) |
CoreLab 測量 tethering/tenting area,但無明確 coaptation length 門檻 | 未規定具體數值 |
| Leaflet mobility (瓣葉活動度) |
排除 leaflet mobility length < 1 cm 須有足夠 mobile leaflet 可供 MitraClip grasping |
CoreLab 評估 leaflet restriction 程度,但無明確數值門檻 | 未規定具體數值 |
| Grasping area 鈣化 | 排除 A2/P2 grasping area 有鈣化 | CoreLab semi-quantitatively 評估鈣化(多切面),但未作為排除條件 | 未明確列出 |
| Grasping area cleft (裂隙) |
排除 A2 或 P2 scallop 有 significant cleft | 未明確列出 | 未明確列出 |
| Chordal support (腱索支撐) |
排除 grasping area 同時缺乏 primary 及 secondary chordal support | 排除 chordal fusion/thickening | 未明確列出 |
| 整體 leaflet anatomy 排除 | 以上 5 項均基於 TEE 評估(180 天內),由 site interventionalist 及 CEC 共同審查 | Abbott proctor 確認 procedural feasibility | 由 investigator 判定 leaflet anatomy 是否 preclude device implantation / positioning / MR reduction |
| 其他解剖條件 | |||
| PASP / 肺高壓 | 排除 PASP > 70 mmHg (例外:vasodilator testing 後 PVR <3 WU,或 PVR 3–4.5 WU 且 v wave < 2× mean PCWP) |
未規定 | 未規定 |
| RV 功能 / TR | 排除 moderate-to-severe RV dysfunction with physical evidence of right-sided HF | CoreLab 評估 TR 分級(4 級 semi-quantitative) | 排除 severe RV failure 或 severe TR |
| Intracardiac mass / thrombus | 排除(echo 及 TEE 評估) | TEE 評估 LA thrombus 及 interatrial septum | 排除 |
| Severe AS / AR / 其他瓣膜病 | 排除 TV/AV disease needing intervention | CoreLab 評估 AS 及 AR severity | 排除 severe AS (AVA <1.0 cm²)、AR、uncorrected severe valve disease |
| Transseptal / vascular access | 明確要求:transseptal catheterisation 及 femoral vein access 均須 feasible | 標準 femoral venous access + transseptal puncture | 未明確列出 |
| Prior MV intervention | 排除:prior MV leaflet surgery、MV prosthesis、prior transcatheter MV procedure | 排除:prior MV repair | 未明確列出 |
| 解剖審查機制 | 三層審查:Site interventionalist(TEE anatomy)→ CEC(GDMT + anatomy + surgical risk)→ Echo core lab(TTE MR severity) v4.1 後 ECL 僅評估 MR severity,TEE anatomy 改由 site 負責 |
Site PI + Abbott proctor 評估 → CoreLab 確認 echo criteria(LVEF, EROA/RVol, 排除 primary MR, 評估 valve anatomy/tethering/calcification) | Site investigator 評估 + Echo core lab 確認 MR severity 及 MVA |
Figure 4. Coaptation Length — mid-systole 時 leaflet 在 atrial-to-ventricular 方向的接觸(或可供接觸)長度,於 four-chamber view 測量。
Source: COAPT Protocol (NEJM Supplement), Appendix A Definitions
COAPT Protocol 以 TEE 為基礎,明確定義五項 leaflet anatomy 排除條件,這是三大 RCT 中最嚴格的解剖篩選: ① Coaptation length ≥ 2 mm(若有 tethering)— 確保 MitraClip 有足夠 tissue 可夾取; ② Leaflet mobility ≥ 1 cm — 確保 leaflet 有足夠活動度供 grasping; ③ 無 grasping area 鈣化 — 鈣化會妨礙 clip 夾合; ④ 無 significant cleft — cleft 會導致 residual MR; ⑤ 須有 primary 或 secondary chordal support — 防止 leaflet avulsion。 相比之下,MITRA-FR 僅由 Abbott proctor 主觀判定 feasibility,RESHAPE-HF2 則由 investigator 自行評估,均未列出量化標準。COAPT 的嚴格解剖篩選是其優異結果的關鍵因素之一——確保入選患者的 MR 確實可被 MitraClip 有效治療。
主要排除條件(Key Exclusion Criteria)
| 排除條件 | COAPT | MITRA-FR | RESHAPE-HF2 |
|---|---|---|---|
| MR / 瓣膜相關 | |||
| Degenerative / Primary MR | 排除(含 flail leaflet) | 排除 primary MR (CoreLab 隨機化前確認) |
排除 degenerative MR(TEE 確認) |
| MVA 過小 | < 4.0 cm² | 未規定 | < 3.0 cm² (3.0–4.0 cm² 可:BSA <2.0 m² 且 gradient ≤3 mmHg) |
| Leaflet anatomy 不適合 | 排除:① mobile leaflet 不足 ② grasping area 鈣化 ③ significant cleft ④ 缺乏 chordal support ⑤ leaflet mobility <1 cm | Abbott proctor 判定不適合 | 排除(investigator 判定) |
| Prior MV intervention | 排除(prior MV surgery/prosthesis/transcatheter procedure) | 排除 prior MV repair | 未明確列出 |
| AV/TV disease | 排除 AV/TV disease 需介入 | 未明確列出 | 排除 severe AS (AVA <1.0 cm²)、AR、uncorrected severe valve disease |
| 血行動力學 / 心室功能 | |||
| PASP / 肺高壓 | > 70 mmHg (例外:vasodilator testing 後 PVR <3 WU,或 3–4.5 WU 且 v wave <2× PCWP) |
未規定 | 未規定 |
| RV dysfunction / TR | 排除 mod-severe RV dysfunction + right-sided HF evidence | 未規定 | 排除 severe RV failure 或 severe TR |
| Stage D / 血行動力學不穩定 | 排除 Stage D HF; SBP <90; 需 inotropes/IABP/MCS | 未明確列出 | 排除 hemodynamic instability requiring inotropic support or MCS 排除 uncontrolled HTN >180/105 或 hypotension SBP <90 |
| LVOT obstruction / HOCM | 排除 HCM | 未明確列出 | 排除 LVOT obstruction、HOCM |
| Restrictive / Infiltrative CM | 排除 HCM, RCM, constrictive pericarditis, amyloidosis, hemochromatosis, sarcoidosis | 未明確列出 | 排除 infiltrative CM(amyloidosis, hemochromatosis, sarcoidosis)、HCM、RCM、constrictive pericarditis、any structural heart disease causing HF other than DCM |
| Washout periods(近期心血管處置) | |||
| Recent MI / ACS | 未明確列出 MI washout (但 CK-MB 須 <ULN 14 天內) |
MI within 3 月 | ACS within 90 天 |
| Recent PCI | within 30 天 | within 1 月 | within 90 天 |
| Recent CABG | within 30 天 | within 3 月 | within 90 天(any CV surgery) |
| Recent CRT / Rhythm device | CRT/CRT-D within 30 天 | CRT within 3 月 | rhythm device implant/revision within 90 天 |
| Recent CVA / TIA / stroke | CVA within 30 天 | stroke within 3 月 | TIA/stroke within 90 天 |
| Recent TAVR | within 30 天 | TAVI within 3 月 | within 90 天(any CV surgery) |
| Recent cardioversion | 未列出 | within 3 月 | 未列出 |
| Recent AF ablation | 未列出 | 未列出 | within 90 天 |
| 新 HF 藥物 | 由 CEC 審查 GDMT 穩定性 | 未明確列出 | 新 drug class 或 dose change within 2 週 |
| 非心臟 / 系統性疾病 | |||
| Untreated CAD | 排除(需 revasc 但未處理) | 未明確列出 | 未明確列出 |
| Severe COPD | 排除(home O₂ 或 chronic oral steroids) | 未明確列出 | 未明確列出 |
| Carotid stenosis | > 70%(severe symptomatic) | 未列出 | 未列出 |
| Renal replacement therapy | 未列出 | 排除(insuffisance rénale terminale — patient dialysé) | 排除(renal replacement therapy) |
| Active infection / endocarditis | 排除 active endocarditis | 排除 active infection(需抗生素治療者) | 排除 active infection 或 endocarditis;排除 rheumatic heart disease |
| Severe hepatic insufficiency | 未列出 | 排除:Factor V <50%(凝血功能障礙之肝功能不全) | 未列出 |
| Bleeding diathesis | 未列出 | 未列出 | 排除 |
| Nitinol hypersensitivity | 未列出 | 排除 | 未列出 |
| IVC filter / DVT | 未列出 | 未列出 | 排除:IVC filter 干擾 delivery catheter 或同側 DVT |
| TEE contraindication | 未列出 | 未列出 | 排除 |
| Transseptal catheterization contraindication | 排除(須確認 transseptal + femoral vein access feasible) | 未列出 | 排除 |
| Medication hypersensitivity | 未列出 | 未列出 | 排除(procedural medications 之已知 hypersensitivity/contraindication 且無法控制) |
| Modified Rankin Scale ≥4 | 排除 | 未列出 | 未列出 |
| Advanced HF / 移植 | |||
| 預期需 LVAD / 心臟移植 | 排除(12 月內預期需 LVAD/transplant) | 排除:autre chirurgie cardiaque programmée(包含登記心臟移植名單) | 排除 Status 1 heart transplant 或 prior orthotopic heart transplantation |
| MV surgery preferred | Heart Team 判定 not appropriate for surgery | Heart Team 判定 non éligible à un geste correcteur par abord chirurgical (至少含 CT surgeon + interventional cardiologist + echocardiographer + anaesthesiologist) |
排除:Heart Team 認為 MV surgery preferred over MitraClip |
| 功能 / 其他 | |||
| 6MWT 上限 | 未設 | 未設 | > 475 m(排除功能太好的患者) |
| Uncontrolled HTN | 未明確列出 | 排除(三階分級): 非糖尿病 >140/90 mmHg 糖尿病/CKD >130/90 mmHg >80 歲 >150 SBP |
排除 >180/105 mmHg 或 SBP <90 mmHg(hypotension) |
| Unstable angina | 未明確列出 | 未明確列出 | 排除 |
| Poorly controlled AF / arrhythmia | 未明確列出 | 未明確列出 | 排除:poorly controlled fast AF/flutter、poorly controlled symptomatic brady-/tachyarrhythmias |
| Life expectancy <12 月 | 排除 | 排除 | 排除 |
| Pregnancy | 排除 | 排除 | 排除 |
| Washout period 總結 | 30 天(最短) | 1–3 月(中等) | 90 天(最長) |
COAPT(NEJM Supplement, 511 頁):共 30 項排除條件(v5.0 最終版),是三試驗中最詳細的。獨有的排除包括:PASP >70 mmHg(搭配 vasodilator testing protocol:PVR <3 WU 或 PVR 3–4.5 WU 且 v wave <2× mean PCWP 方可例外)、moderate-severe RV dysfunction with right-sided HF、5 項定量 leaflet anatomy criteria、untreated CAD needing revascularization、severe COPD(home O₂ or chronic oral steroids)、carotid stenosis >70%、Modified Rankin Scale ≥4。CEC 三層審查篩掉約 34% 患者。
MITRA-FR(Version 15, 法文, 187 頁):排除條件短但有獨特規定——uncontrolled HTN 採三階分級標準(非糖尿病 >140/90、糖尿病/CKD >130/90、>80 歲 >150 SBP),嚴重肝功能不全以 Factor V <50%(非 Child-Pugh)定義,另排除 nitinol 過敏和 cardioversion 3 月內。CoreLab(Hôpital Bichat)隨機化前確認 echo criteria 並排除 primary MR。
RESHAPE-HF2(Version 6.0, 236 頁):排除條件覆蓋面最廣但定義最彈性——獨家排除 IVC filter 干擾 delivery catheter、TEE contraindication、transseptal catheterization contraindication、active rheumatic heart disease、poorly controlled fast AF/flutter、poorly controlled brady-/tachyarrhythmias、unstable angina、bleeding diathesis、procedural medication hypersensitivity。90 天最長 washout period 確保病情穩定。
Supplementary Appendix 揭示一項重要但常被忽略的細節:COAPT 的 BNP 門檻經 BMI 校正——BMI 超過 20 kg/m² 時,BNP cutoff 每增加 1 kg/m² 降低 4%(例如 BMI 30 的患者,BNP cutoff 約 180 pg/mL 而非 300)。這反映了肥胖患者 BNP 偏低的生理特性,確保不因 BMI 而漏收真正的 HF 患者。
三試驗 HF 住院要求截然不同:MITRA-FR 是唯一將 HF 住院列為必要條件(12 月內至少 1 次,無 BNP 替代選項),意味著 100% 入組者都有 HF 住院史。COAPT 允許 BNP/NT-proBNP 作為替代(corrected BNP ≥300 或 NT-proBNP ≥1500),RESHAPE-HF2 門檻更低(NT-proBNP ≥1000)。這些差異直接影響入組患者的疾病嚴重度和 event rate。
三試驗的 washout period 從 COAPT 的 30 天、MITRA-FR 的 1–3 月、到 RESHAPE-HF2 的 90 天 遞增。RESHAPE-HF2 更獨家要求隨機化前 2 週內不可有新 HF drug class 或 dose change——這確保入組時 GDMT 已真正穩定,而非仍在 uptitration 過程中。
RESHAPE-HF2 獨有的 6MWT > 475 m 排除標準從上界排除功能太好的患者,搭配 NYHA ≥II 和 HF 住院/BNP 要求形成精巧的雙向篩選。COAPT 則以 Modified Rankin Scale ≥4(嚴重失能)和 Stage D HF 排除下界。每個試驗都在定義自己的「sweet spot」患者群。
COAPT 的「嚴格篩選」策略是三大 RCT 差異的核心。COAPT 有兩道獨特品質門檻:(1) Echo core lab 以 3-tier multiparametric algorithm 確認 MR 嚴重度(Iung et al., Circulation 2020);(2) CEC 逐案審查 GDMT 優化程度、解剖適合性和手術風險,篩掉約 34% 的患者。COAPT 還獨家要求 LVESD ≤70 mm、CK-MB <ULN、transseptal/femoral access feasibility。
MR 嚴重度的實際差距:COAPT mean EROA 0.41 cm²(core lab 確認),遠高於 MITRA-FR(0.31 cm²)和 RESHAPE-HF2(median 0.23 cm²)。搭配較小的 LVEDV(193 mL),COAPT 患者代表典型的「disproportionate MR」——MR 對心衰的貢獻超過 LV 擴張所預期,修復 MR 的邊際效益最大。
Echo Core Lab 角色的重新理解:Supplementary Appendices 揭示三個試驗都有 core lab 參與,但角色不同。COAPT:core lab 確認 MR severity(3-tier algorithm);MITRA-FR:CoreLab 隨機化前確認 LVEF、EROA/RVol、排除 primary MR(Protocol);RESHAPE-HF2:core lab 確認 MR severity 及 MVA。差異在於 COAPT 的 core lab 使用更嚴格的 MR severity 定義(multiparametric 而非單一 EROA/RVol cutoff)。
ESC 2025 Class I, Level A 建議的實證基礎,來自符合 COAPT-like 收案標準的患者。綜合三份 Supplementary Appendices 的完整收排條件,臨床上選擇 TEER 候選人時應確認:
① 真正的 severe MR(EROA ≥0.3 cm² 或 RVol ≥45 mL,最好由心超專家或 core lab 確認)
② 穩定的最大耐受劑量 GDMT(包括 ARNI, beta-blocker, MRA, ± SGLT2i, ± CRT);RESHAPE-HF2 要求至少 2 週無 dose change
③ LVESD ≤70 mm、LVEDV 不過大(COAPT LVESD 上限為 70 mm;LVEDV <200 mL 為 sweet spot)
④ 無嚴重 RV dysfunction 或 severe TR;PASP ≤70 mmHg
⑤ MVA 足夠(COAPT ≥4.0 cm²;RESHAPE-HF2 ≥3.0 cm²;避免 clip 後 MS)
⑥ Heart Team 多學科評估,含解剖適合性審查
RESHAPE-HF2 的意義在於擴展了 TEER 的適用範圍至 moderate-to-severe MR(EROA 0.2–0.3 cm²),但 COAPT-like severe MR 仍是獲益最確定的族群。在 moderate SMR 區間,仍需更多數據(如 MATTERHORN 的 subgroup 分析、進行中的 IPD meta-analysis)來釐清最佳患者篩選策略。
RESHAPE-HF2 的患者 EROA 更小(median 0.23 cm²)、LVEDV 介於 COAPT 和 MITRA-FR 之間(median 200 mL),LVEF median 31–32%,代表一個更「真實世界」的人群。結果顯示 TEER 在 moderate-to-severe FMR 中也有效,但死亡率未達統計顯著——可能反映較低風險的族群[7]。
Stone 在 JACC editorial 中稱 RESHAPE-HF2「消除了所有疑慮」,將 MITRA-FR 定位為「outlier trial」[6]。但 MITRA-FR PI Obadia 質疑其為「tiebreaker」的地位,指出多重 endpoint 修改和試驗設計問題[6]。
ESC/EACTS 2025 Guideline 建議
| 情境 | 建議 | Class | LOE | 較 2021 年變化 |
|---|---|---|---|---|
| Severe V-SMR + HF + LVEF <50% (optimized GDMT 後仍有症狀) |
TEER 以降低 HFH 並改善生活品質 | I | A | ⬆️ 從 IIa/C 升至 I/A |
| Atrial SMR (不適合手術者) |
可考慮 TEER | IIb | B | 🆕 新增建議 |
| Atrial SMR (可手術者) |
手術修復 ± AF ablation ± LAA closure | IIa | B | 🆕 新增建議 |
| V-SMR + HF 需手術治療 | 外科 MV repair/replacement | I | C | 維持不變 |
TEER 在 severe V-SMR 中從 Class IIa 升至 Class I, Level A — 這是基於三項 RCT 的 meta-analysis:HF 再住院 HR 0.63 (0.50–0.80),複合終點(死亡 + 全因住院)HR 0.72 (0.51–0.999)[8]。Borger(EACTS chair)指出:「我們也首次在任何指引或共識文件中明確定義了 atrial secondary MR」[8]。此外,MATTERHORN 結果也被納入(ref 617),支持 TEER 在 V-SMR 中對手術的 noninferiority。
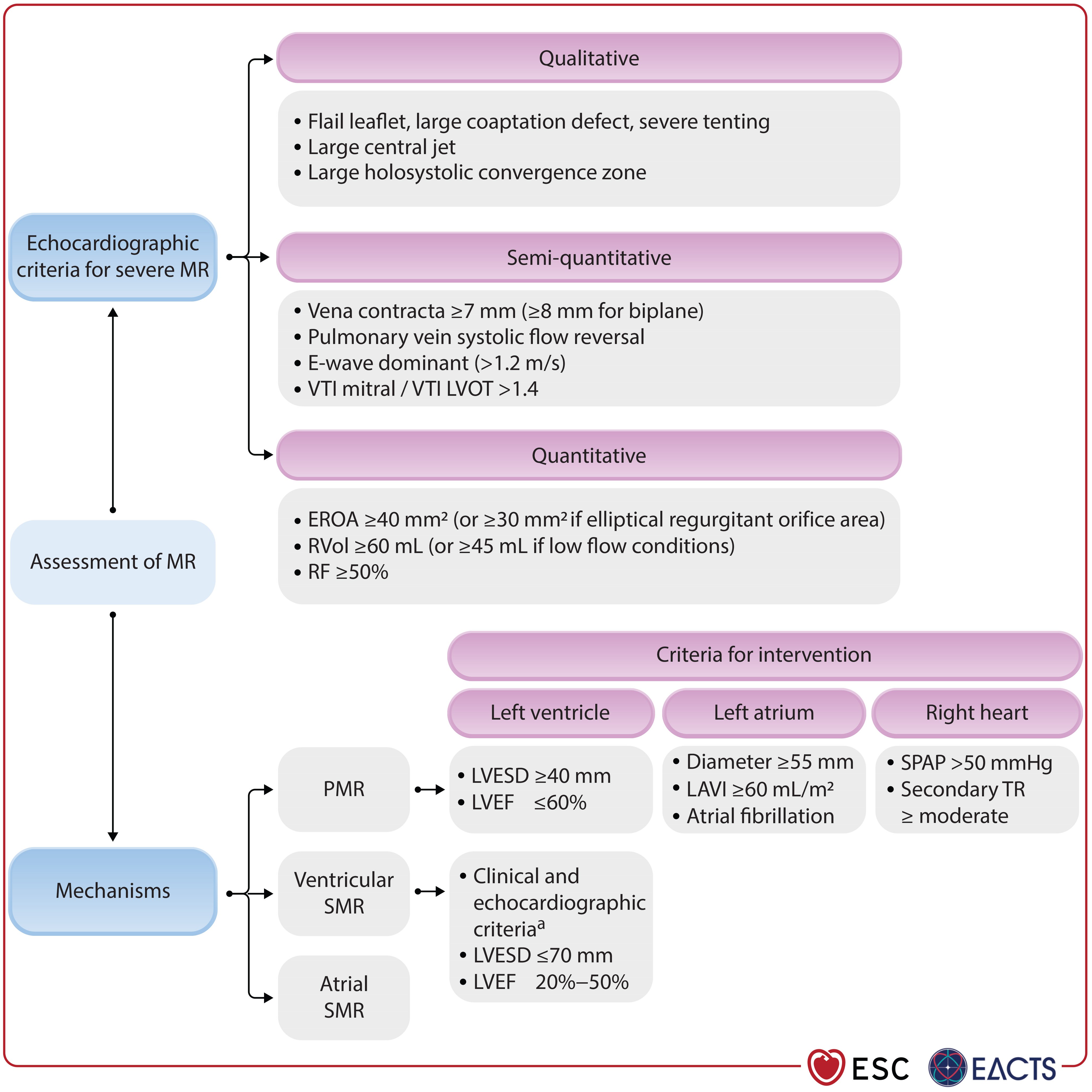
ESC 2025 Table 7:M-TEER 適應症標準(Recommendation Table 7)
| 條件 | 標準 |
|---|---|
| MR 嚴重度 | Severe secondary MR(optimized GDMT 後仍存在) |
| LVEF | 20–50% |
| LVESD | ≤70 mm |
| NYHA class | ≥ II |
| HF hospitalization | ≥1 次 HF 住院於 過去 1 年內,或 BNP ≥300 pg/mL / NT-proBNP ≥1000 pg/mL |
| 肺動脈壓力 | SPAP ≤70 mmHg |
| RV 功能 | 無嚴重 RV dysfunction |
| 排除條件 | Stage D / advanced HF;需要血管重建的 CAD |
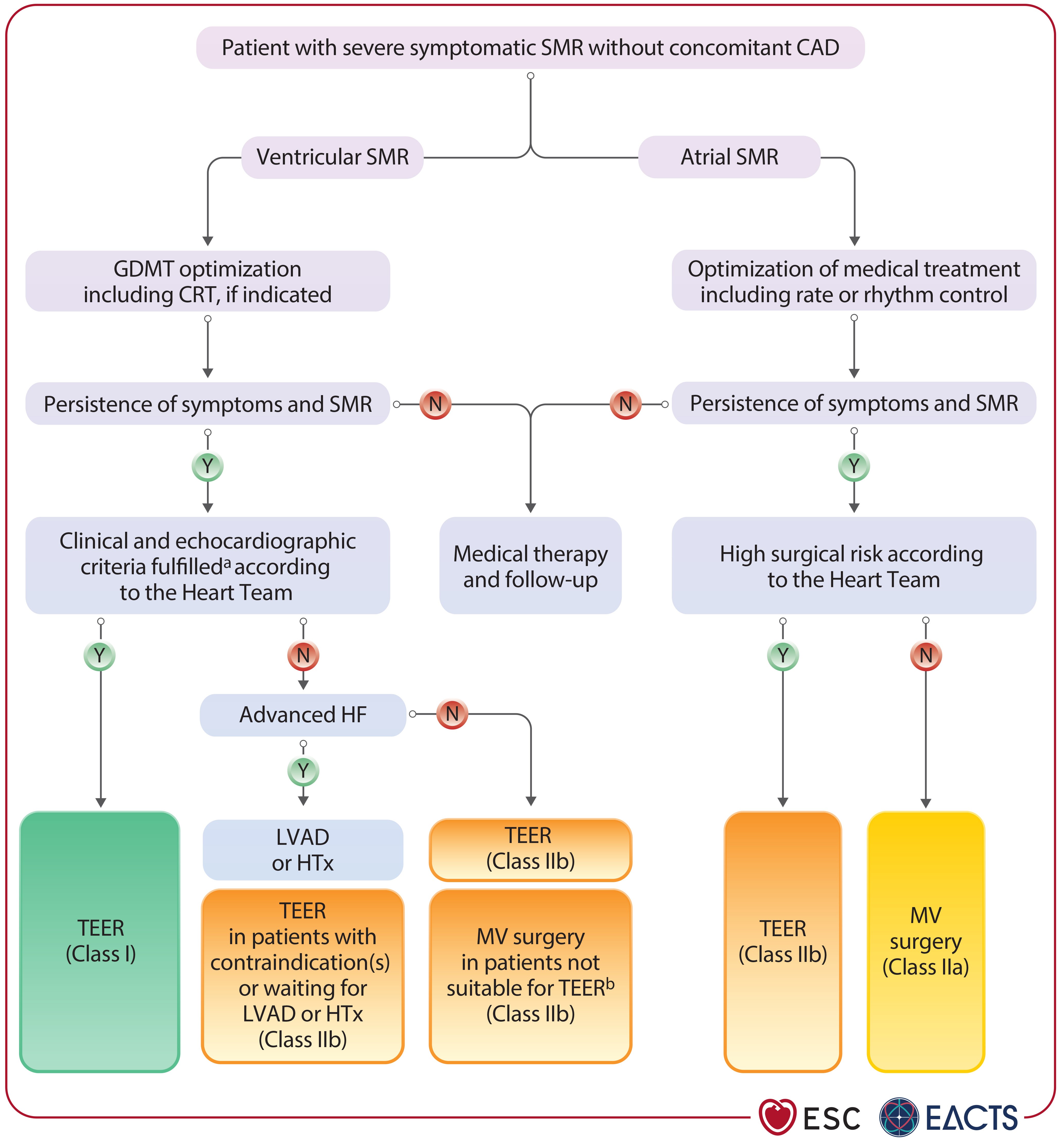
ESC 2025 Table 7 標準比 COAPT 更寬鬆:LVEF 範圍擴展至 20–50%(COAPT 為 20–50%),但新增了 LVESD ≤70 mm 和 SPAP ≤70 mmHg 的限制,並要求排除需要冠狀動脈血管重建的患者。關鍵的是,指引明確要求「在無需血管重建的有症狀患者中,建議 M-TEER」[8]。
病人篩選:誰最可能獲益?
有利預後因子(TEER 後獲益較大)
基於 EuroIntervention 2025 SOTA review 及多項登記研究[4]:
| 預後因子 | 有利 | 不利 |
|---|---|---|
| MR 嚴重度 | Severe(EROA ≥0.30 cm²) | Moderate(EROA <0.20 cm²;證據有限) |
| LV 大小 | LVEDV <200 mL(disproportionate) | LVEDV >250 mL(proportionate) |
| RV 功能 | TAPSE 保存 | TAPSE <17 mm,RV dysfunction |
| Staging | Stage 1–2(isolated MV/LV involvement) | Stage 3–4(RV overload/biventricular failure) |
| TR 嚴重度 | 輕度或無 TR | Severe TR(獨立預後不良因子) |
| Pulmonary HTN | 無或輕度 | 嚴重 PH(獨立增加死亡風險) |
| GDMT 使用 | 已最佳化四柱 GDMT | GDMT 尚未優化(先優化再評估) |
| 術後 GDMT 加強 | TEER 後持續 uptitrate GDMT | 術後未調整 GDMT |
SMR Staging System(Stolz et al.)
一個四階段分期系統已被提出,用於評估 extramitral cardiac involvement[4]:
| Stage | 定義 | 2 年死亡率 |
|---|---|---|
| Stage 1 | Isolated MV disease | 最低 |
| Stage 2 | MV + LV involvement | 中等 |
| Stage 3 | + RV pressure/volume overload | 顯著升高 |
| Stage 4 | Biventricular failure | 最高 |
介入前的必要步驟:GDMT 優化
目前所有指引一致建議:在考慮 TEER 之前,必須先完成 GDMT 全面優化[4,8]。這包括:
| 治療 | 目標 | 對 SMR 的影響 |
|---|---|---|
| ACEi/ARB → ARNI | 最大耐受劑量 | Sacubitril/valsartan:EROA ↓34.6%;~50% severe→non-severe |
| Beta-blocker | 最大耐受劑量 | Reverse remodeling → 改善 coaptation |
| MRA | 標準劑量 | 減少 volume overload |
| SGLT2i | 標準劑量 | 新證據顯示可減少 functional MR |
| CRT(若符合適應症) | LBBB + LVEF ≤35% | Resynchronization → reverse remodeling → MR↓ |
TCTMD 報導了一項觀點[9]:在現代四柱 GDMT 之下,SGLT2i 對 SMR 的改善可能足以「取代」部分 TEER 的需求。然而,三大 RCT 均在 SGLT2i 廣泛使用前完成,目前缺乏「四柱 GDMT + TEER」vs「四柱 GDMT alone」的 head-to-head 比較。EuroIntervention 2025 SOTA 特別強調:TEER 後持續 GDMT uptitration 的組合策略獲益最大[4]。
介入時機的關鍵考量
不要太晚:等到 stage 3–4(RV dysfunction/biventricular failure)才介入,預後顯著惡化[4]。MITRA-FR 的啟示是,嚴重 LV 擴大(LVEDV >250 mL)可能意味著「too late」。
不要太早:GDMT 優化需要時間(通常 3–6 個月),~60% 患者在 GDMT 後 SMR 會改善。過早介入可能進行不必要的手術。
最佳時間窗:GDMT 優化 ≥3 個月後,若 SMR 仍為 severe(≥3+)且患者持續有症狀(NYHA ≥II),應轉介 Heart Team 評估 TEER[8]。
EuroSMR registry 資料顯示,TEER 後持續 GDMT uptitration 的患者有更好的長期存活率,即使在 RV dysfunction 亞組中也是如此[4]。TEER 不是 GDMT 的替代品,而是互補的治療策略。Stone 提到 COAPT 中 TEER 的 NNT 比任何單一 HF 藥物都低,但他也強調需要更早思考介入時機[6]。
Moderate SMR:要不要提早介入?
RESHAPE-HF2 的患者 median EROA 僅 0.23 cm²(只有 14% EROA >0.40 cm²),代表許多是 moderate-to-severe 而非嚴格的 severe MR。結果仍顯示 TEER 有效。Anker 表示:「我認為我們確認了 severe MR 的結果;對於 less than severe,這是好的跡象,但需要驗證」[6]。
JACC 2025 專文探討了 moderate SMR 的治療策略[10],EuroIntervention editorial 也呼籲擴展 TEER 適應症至 moderate SMR[11]。但目前指引尚未納入此建議——需要專門的 RCT 驗證。
治療策略總覽
| 治療 | 適應症 | Class/LOE (ESC 2025) | 實證等級 |
|---|---|---|---|
| TEER(MitraClip / PASCAL) | Severe V-SMR, HF, LVEF <50%, optimized GDMT | I / A | Landmark RCT |
| 外科 MV repair/replacement | V-SMR 需同時進行 CABG/其他心臟手術 | I / C | Observational |
| 外科 MV repair | A-SMR 可手術者 ± AF ablation | IIa / B | RCT |
| TEER for A-SMR | A-SMR 不可手術者 | IIb / B | Registry |
| GDMT(四柱) | 所有 HFrEF + SMR(基礎治療) | I / A | Landmark RCT |
| CRT | LBBB + LVEF ≤35% + optimized GDMT | I / A | Landmark RCT |
TEER:目前的標準
MitraClip System
MitraClip 是目前證據最充分的 TEER device。從 EVEREST II(2013)到 COAPT(2018)、RESHAPE-HF2(2024),歷經迭代改良——包括 independent leaflet grasping 和擴大的 device sizes(NTR/XTR/G4)[12]。MitraClip G4 系統進一步改善了操控性和適用範圍。
PASCAL System
PASCAL 系統具有更寬的 paddles 和獨特的 grasping mechanism,在 CLASP IID/IIF 試驗中顯示對 MitraClip 的 noninferiority[12]。對於某些解剖型態(如 large coaptation gap),PASCAL 可能提供更好的 MR reduction。
TEER vs 手術:MATTERHORN(NEJM 2024)
MATTERHORN 是第一個直接比較 TEER 與外科手術治療 SMR 的 RCT[13]。210 名患者(HF + severe SMR, mean LVEF 43.0±11.7%, 53% annular dilatation / 47% ventricular tethering)隨機分配至 MitraClip(n=104)或手術(n=106)。值得注意的是,~48% 患者 LVEF >40%,EuroSCORE II 僅 3.0%,且 82.9% 曾於 1 年內因 HF 住院。
| 終點 | TEER | 手術 | 差異 |
|---|---|---|---|
| Primary efficacy composite (death, HFH, reintervention, LVAD, stroke) |
16.7% | 22.5% | -6% (CI -17 to 6%) 達到 noninferiority |
| Primary safety | 14.9% | 54.8% | -40% (CI -51 to -27%) TEER 顯著更安全 |
| MR 3–4+ 復發率 | 8.9% | 1.5% | 手術 MR reduction 更持久 |
| 住院天數 | 4 天 | 12 天 | TEER 恢復更快 |
| ICU 天數 | 1 天 | 3 天 | — |
| 死亡(secondary endpoint) | — | — | HR 0.61 (0.24–1.57) NS |
Chikwe(心臟外科醫師)批評[14]:(1) 沒有 medical arm;(2) noninferiority margin 17.5% 過於寬鬆;(3) 複合終點偏向不利手術(包含常見的術後暫時性併發症);(4) ~48% 患者 LVEF >40%,限制了對典型 HFrEF 的推論。Messika-Zeitoun 更直言:「缺乏標準治療對照組,他們只是證明了不需要做的手術可能會致命」[14]。
未來方向
Transcatheter MV Replacement (TMVR):包括 Tendyne(SUMMIT 試驗)和 Intrepid(APOLLO 試驗),適用於不適合 TEER 的患者(leaflet tethering、annular calcification)。但 LVOTO 風險、device anchoring 和耐久性仍是挑戰[12]。
Annuloplasty-based interventions:Carillon(coronary sinus-based)和 AccuCinch(LV reshaping)可能作為 TEER 的輔助或橋接治療[12]。
需要的 RCT:(1) 四柱 GDMT + TEER vs 四柱 GDMT alone;(2) Moderate SMR 的 dedicated RCT;(3) COAPT/MITRA-FR/RESHAPE-HF2 的 IPD meta-analysis(Anker 已承諾分享資料,但 COAPT 資料的取得仍待確認)[6]。
Expert Perspectives:共識與爭議
ESC 2024 同時發表 RESHAPE-HF2 和 MATTERHORN 兩項重磅試驗後,學界反應兩極化。JACC 一口氣刊登了主文、三篇 editorial、一篇 meta-analysis 和一篇 substudy,反映出這個議題的高度爭議性。以下依「支持 TEER」、「質疑 TEER」、「中立/理論框架」和「ESC 2025 指引觀點」分層整理。
🟢 支持 TEER 的聲音
| 專家 / 來源 | 身份 | 核心論點與關鍵引述 |
|---|---|---|
| Gregg W. Stone | COAPT PI Icahn School of Medicine at Mount Sinai |
JACC Editorial 標題即立場:「M-TEER for Functional MR: Erasing All Doubt」[6,21] ① RESHAPE-HF2 確認 COAPT 結果,讓 MITRA-FR 成為「outlier trial」 ② TEER 的 NNT(number needed to treat)低於任何單一 HF 藥物 ③ 呼籲更早考慮介入:不應等到患者病程已至晚期才轉介 ④ 指出三試驗 meta-analysis 顯示 HFH 和複合終點均達統計顯著 |
| Stefan D. Anker | RESHAPE-HF2 PI Charité – Universitätsmedizin Berlin |
① 確認 severe MR 的 TEER 獲益 ② 對 moderate MR 的結果審慎樂觀:「這是好的跡象,但需要驗證」[6] ③ 反對將 TEER 稱為 HF 的「第五根支柱(pillar)」——認為言過其實 ④ 承諾分享 RESHAPE-HF2 individual patient data 用於 IPD meta-analysis ⑤ RESHAPE-HF2 的 co-primary endpoints 涵蓋 HFH+CV death(RR 0.64)、單純 HFH(RR 0.59)、及 KCCQ(Δ10.9 points),三者同時陽性增強結論可信度 |
| Stephan Baldus | MATTERHORN PI University of Cologne |
MATTERHORN 證實 TEER 在 1 年 efficacy 上不劣於手術,且 30 天 safety 顯著更佳(14.9% vs 54.8%)[13] TEER 住院天數 4 vs 12 天、ICU 1 vs 3 天——對高齡 HF 患者而言,減少侵入性創傷意義重大 |
| Fabien Praz | ESC 2025 VHD Guideline Chair Bern University Hospital |
TEER 升級為 Class I/A 是「對於在 optimized GDMT 和 CRT 後仍有症狀的患者的重大進展」[8,15] 指引首次明確區分 V-SMR 和 A-SMR,並為兩者分別提供管理建議 |
🔴 質疑 TEER 的聲音
| 專家 / 來源 | 身份 | 核心論點與關鍵引述 |
|---|---|---|
| Jean-François Obadia | MITRA-FR PI Hôpital Louis Pradel, Lyon |
JACC Editorial 標題:「Plea for an In-Depth Analysis of the RESHAPE-HF2 Results」[22] ① RESHAPE-HF2 不是「tiebreaker」——試驗有以下缺陷: • 原始 primary endpoint 被修改(從 2 年 HFH+CV death 擴展為三個 co-primary endpoints) • 試驗持續時間過長(2018 啟動,2024 才發表),期間多次 protocol amendment • Liberal endpoint definitions 增加 false positive 風險 • Control 組非 CV 住院率意外偏高,需要額外調查 ② 結論:「RESHAPE-HF2 不會終結辯論;相反,它最大的貢獻是重新激發了這場討論」[22] ③ 需要 IPD meta-analysis 才能真正識別獲益亞群 |
| Nathan Mewton | MITRA-FR Senior Investigator Hôpital Cardiovasculaire Louis Pradel |
① 核心質疑:HFH 顯著降低卻完全沒有死亡率趨勢——「When you have a very significant impact on heart failure hospitalization, you should at least have a trace towards improvement in mortality, especially with a follow-up of 2 years」[6] ② RESHAPE-HF2 試驗存在多項可疑之處:延遲的入組、反覆的 endpoint 修改、過時的背景 GDMT(SGLT2i 使用率極低) ③ 德國站點缺乏 equipoise(隨機分配到 control 組的患者可能不被接受),大部分患者來自波蘭和希臘 ④ 隨機化後的藥物調整資訊缺失——無法確認兩組 GDMT 是否等同 |
| Joanna Chikwe & Michelle Kittleson | NEJM Editorial Cedars-Sinai Medical Center |
NEJM Editorial 標題:「Transcatheter Repair or Surgery for Functional Mitral Regurgitation」[23] ① SMR 本質是「ventricular disease with very poor survival」,修復二尖瓣是「a long-shot approach」 ② MATTERHORN 的核心缺陷:沒有 medical control arm——「The standard of care should have been medical, and there is no medical group」 ③ Noninferiority margin 17.5% 過於寬鬆 ④ 30 天 safety composite 偏向不利手術(包含新發 AF 33% vs 9%——術後常見且通常可逆的併發症) ⑤ ~48% 患者 LVEF >40%,限制了對典型 HFrEF 人群的推論 |
| David Messika-Zeitoun | University of Ottawa Heart Institute |
批評 MATTERHORN 最直接的聲音:「缺乏標準治療對照組,他們只是證明了不需要做的手術可能會致命」[14] 質疑在目前已有 COAPT 級別證據支持 TEER vs GDMT 的情況下,為何還要比較 TEER vs 手術——而非驗證 TEER vs 最佳藥物治療 |
🟡 中立 / 理論框架
| 專家 / 來源 | 身份 | 核心論點與關鍵引述 |
|---|---|---|
| Harlan Krumholz | JACC Editor-in-Chief Yale School of Medicine |
以 JACC EIC 身份,在同一期刊登 Stone 的支持 editorial 和 Obadia 的批評 editorial——體現學術公正[6] 觀察到:「你幾乎可以根據自己的立場看到想看的結果(you can almost see what you want to see based on your position)」 呼籲 IPD meta-analysis 才能真正解決爭議 |
| Aakriti Gupta, Milton Packer, Raj Makkar, Paul Grayburn |
JACC Editorial Cedars-Sinai + Baylor |
JACC Editorial:「A Volume-Based Framework Reconciling COAPT, MITRA-FR, and RESHAPE-HF2」[19] ① LVEDV 是調和三試驗結果的統一變量:COAPT(193 mL)→ 最大獲益;RESHAPE-HF2(200 mL)→ 中間獲益;MITRA-FR(~260 mL)→ 無獲益 ② 當 LVEDV 超過臨界值,MitraClip 減少 MR 的能力不足以改變臨床結局 ③ 此框架延伸了 Grayburn 2019 的 proportionate/disproportionate 概念[5],但更實用——用絕對 LVEDV 而非 EROA/LVEDV 比值來預測獲益 |
| 三試驗 Meta-analysis (JACC 2024) |
Pooled analysis COAPT + MITRA-FR + RESHAPE-HF2 |
Pooled n = 1,426[24]: • HF 住院:HR 0.63 (0.50–0.80) ✓ • 全因死亡:HR 0.76 (0.57–1.01) — 邊界未達顯著 • CV 死亡:HR 0.77 (0.56–1.06) — 同樣邊界未達顯著 作者結論:「an individual patient-level meta-analysis is urgently needed」以釐清異質性來源 |
🔵 ESC/EACTS 2025 指引觀點
| 專家 | 身份 | 核心論點 |
|---|---|---|
| Michael Borger | EACTS Chair Leipzig Heart Center |
① 「我們也首次在任何指引或共識文件中明確定義了 atrial secondary MR」[8] ② 希望此定義成為未來的標準 ③ 指引整體方向是「更早、更以證據為基礎的介入,以及更以病人為中心的創新」 |
| Fabien Praz | ESC Chair Bern University Hospital |
① TEER 升至 Class I/A 是基於三項 RCT 的一致方向性結果,加上 meta-analysis 支持 ② 明確要求:「在無需冠脈血管重建的有症狀患者中,建議 M-TEER」[8] ③ 同時承認 MATTERHORN 結果(TEER 對手術 noninferiority),納入指引考量 |
這場辯論的深層分歧在於對 SMR 本質的不同理解。Interventional cardiologists(Stone、Anker)將 SMR 視為一個可獨立干預的治療靶點——打斷 volume overload 惡性循環即可改善預後。Surgeons 和 HF specialists(Chikwe、Obadia、Mewton)則視 SMR 為心室疾病的下游表現——處理瓣膜並不能改變根本的心肌病變。
ESC 2025 的裁決(Class I/A)傾向前者,但附加了嚴格的病人篩選標準(Table 7),實質上承認了後者的擔憂:並非所有 SMR 患者都適合 TEER。Krumholz 的觀察最為精闢:這些數據足夠讓兩方都看到自己想看的結論,唯有 IPD meta-analysis 才能最終解答「who benefits and why」。
從支持者學到的:TEER 在精選患者中的獲益是真實且可重複的(COAPT + RESHAPE-HF2),ESC 已認可這一點。三試驗 meta-analysis 的 HFH HR 0.63 提供了群體層面的信心。
從質疑者學到的:死亡率獲益仍未確立(pooled HR 0.76, CI crossing 1.0)。RESHAPE-HF2 的 endpoint 修改和 MATTERHORN 缺乏 medical arm 是真實的方法學缺陷,不應被忽視。病人篩選至關重要——LVEDV >250 mL 的 proportionate MR 可能不適合 TEER。
未解之問:① 現代四柱 GDMT 下 TEER 的增量效益?② Moderate SMR 是否也應介入?③ IPD meta-analysis 何時完成?④ TEER 對手術的長期(>1 年)比較?
Ongoing Trials(進行中的重要試驗)
| 試驗 | 人群 | 介入 | 主要終點 |
|---|---|---|---|
| REPAIR MR | Severe PMR, moderate surgical risk | TEER (MitraClip) vs late surgery | Death, stroke, CV hosp, MR reduction |
| SUMMIT | Symptomatic ≥moderate-severe MR | Tendyne TMVR vs MitraClip | Death or HFH at 1 yr |
| APOLLO | Severe symptomatic MR | Intrepid TMVR vs GDMT | Death or HFH at 1 yr |
| EMPOWER | HF + ≥mild FMR | Carillon annuloplasty vs GDMT | Death, major AE at 2 yr |
| IPD Meta-analysis (COAPT + MITRA-FR + RESHAPE-HF2) |
Pooled individual data | — | Identify optimal patient subgroups |
1. TEER is now Class I:ESC 2025 將 TEER 升為 Class I/A,對 severe V-SMR 而言已是標準治療,不再只是「可考慮」。
2. Patient selection is everything:Disproportionate MR(EROA 大、LV 不太大)獲益最大;Stage 3–4 預後差但仍可能獲益;GDMT 必須先優化。
3. TEER + GDMT, not TEER vs GDMT:TEER 和現代四柱 GDMT 是互補的;術後持續 GDMT uptitration 是最佳策略。未來需要「四柱 GDMT + TEER」的 dedicated RCT。
References
- Bartko PE, et al. Burden, treatment use, and outcome of secondary mitral regurgitation across the spectrum of heart failure. BMJ. 2020;373:m1455.
- Goliasch G, et al. Prevalence and Prognostic Significance of Mitral Regurgitation in Acute Decompensated Heart Failure: The ARIC Study. JACC Heart Fail. 2021;9(3):179-189.
- Dziadzko V, et al. Outcome and undertreatment of mitral regurgitation: a community cohort study. Lancet. 2018;391:960-969.
- Rodés-Cabau J, Mengi S, Salaun E, Paradis JM, Abraham WT. Transcatheter edge-to-edge repair in secondary mitral regurgitation. EuroIntervention. 2025;21:e1458-e1478. DOI: 10.4244/EIJ-D-25-00116.
- Grayburn PA, Sannino A, Packer M. Proportionate and disproportionate functional mitral regurgitation: a new conceptual framework that reconciles the results of the MITRA-FR and COAPT trials. JACC Cardiovasc Imaging. 2019;12(2):353-362. DOI: 10.1016/j.jcmg.2018.11.006.
- Wood S. RESHAPE-HF2 Is a Win for MitraClip in FMR—Not Everyone's On Board. TCTMD. August 31, 2024.
- Anker SD, Friede T, von Bardeleben RS, et al. Transcatheter valve repair in heart failure with moderate to severe mitral regurgitation. N Engl J Med. 2024;391(19):1799-1809. DOI: 10.1056/NEJMoa2314328 (RESHAPE-HF2).
- Praz F, Borger MA, Lanz J, et al. 2025 ESC/EACTS Guidelines for the management of valvular heart disease. Eur Heart J. 2025;46(44):4635–4765. DOI: 10.1093/eurheartj/ehaf194.
- O'Riordan M. SGLT2 Inhibitor Added to GDMT in Functional MR May Obviate Need for TEER. TCTMD. May 7, 2024.
- Moderate Secondary Mitral Regurgitation: Evolving Evidence and Management Strategies. JACC. 2025.
- Expanding the boundaries of M-TEER: is it time to treat moderate secondary mitral regurgitation? EuroIntervention. 2024.
- Binder C, Siegel RJ. Advancing the Management of Mitral Regurgitation: A New Era of Personalization and Innovation. ACC.org Expert Analysis. June 2, 2025.
- Baldus S, Doenst T, Pfister R, et al. Transcatheter repair versus mitral-valve surgery for secondary mitral regurgitation. N Engl J Med. 2024;391:1787-1798. DOI: 10.1056/NEJMoa2408739 (MATTERHORN).
- Wood S. MitraClip vs Surgery for Severe FMR? MATTERHORN Claims Noninferiority. TCTMD. September 1, 2024.
- Maxwell YL. ESC/EACTS Release New Valvular Heart Disease Guidelines. TCTMD. September 3, 2025.
- Stone GW, Abraham WT, Lindenfeld J, et al. Five-year follow-up after transcatheter repair of secondary mitral regurgitation. N Engl J Med. 2023;388:2037-2048 (COAPT 5-year).
- Obadia JF, Messika-Zeitoun D, Leurent G, et al. Percutaneous repair or medical treatment for secondary mitral regurgitation. N Engl J Med. 2018;379:2297-2306 (MITRA-FR).
- Stone GW, Lindenfeld J, Abraham WT, et al. Transcatheter mitral-valve repair in patients with heart failure. N Engl J Med. 2018;379:2307-2318 (COAPT).
- Gupta A, Packer M, Makkar R, Grayburn PA. A volume-based framework reconciling COAPT, MITRA-FR, and RESHAPE-HF2. J Am Coll Cardiol. 2024;84(19):1875-1880. DOI: 10.1016/j.jacc.2024.08.029.
- Stolz L, et al. Staging system for secondary mitral regurgitation. EuroIntervention. 2024.
- Stone GW, Penta B. M-TEER for functional MR: erasing all doubt. J Am Coll Cardiol. 2024;84(19):1881-1884. DOI: 10.1016/j.jacc.2024.08.037.
- Obadia JF, Mewton N, Music S, et al. Plea for an in-depth analysis of the RESHAPE-HF2 results. J Am Coll Cardiol. 2024;84(19):1885-1889. DOI: 10.1016/j.jacc.2024.08.030.
- Chikwe J, Kittleson MM. Transcatheter repair or surgery for functional mitral regurgitation. N Engl J Med. 2024;391(19):1850-1851. DOI: 10.1056/NEJMe2411217.
- Grinfeld L, Raposeiras-Roubín S, Pibarot P, et al. Percutaneous transcatheter edge-to-edge repair for functional mitral regurgitation in heart failure: a meta-analysis of 3 randomized controlled trials. J Am Coll Cardiol. 2024;84(19):1862-1874. DOI: 10.1016/j.jacc.2024.08.026.