1. 引言:ISR 仍然是 PCI 的阿基里斯腱
In-stent restenosis(ISR)是經皮冠狀動脈介入治療(percutaneous coronary intervention, PCI)後最常見的支架失效原因。[1,2] 儘管新世代藥物洗脫支架(drug-eluting stent, DES)大幅降低了再狹窄率,ISR 仍佔所有 PCI 的 5–10%:美國估計約 10%,歐洲約 5%。[1,3] 在絕對數量上,由於每年全球 PCI 量持續增長,ISR-PCI 的總量反而呈上升趨勢。[3]
定義: ISR 傳統上定義為先前支架範圍(含支架外緣 5 mm,即「stent edges」)的管腔直徑狹窄 ≥50%,結合血管造影或 intravascular imaging(IVI)評估。[1,2] 「Clinical restenosis」則指 ISR 合併症狀或缺血證據。值得注意的是,並非所有 ISR 都會產生症狀——相當比例為「silent restenosis」,這也是長期追蹤的重要考量。[2]
ISR 不是一個均一的疾病。它涵蓋多種病理機制(neointimal hyperplasia、neoatherosclerosis、mechanical failure),臨床表現從穩定型心絞痛到急性冠心症(ACS)皆可能。在 DES-ISR 的病患中,高達 20% 以 ACS 方式呈現,伴隨相對應的 morbidity 與 mortality。[1,2]
2. 機制與分類
2A. 病理機制
ISR 的病理機制可歸納為三大類因素:extra-stent factors(支架外因素,如多層支架、血管鈣化、vessel size)、stent-related factors(支架因素,如 underexpansion、fracture、geographic miss)、以及 intra-stent factors(支架內因素,如 neointimal hyperplasia、neoatherosclerosis)。這些因素常共存,在治療 ISR 時需全面評估。[2,4]
Neointimal Hyperplasia (NIH)
NIH 是 ISR 最傳統的機制,源自平滑肌細胞增生與細胞外基質堆積。在 BMS-ISR,NIH 是絕對主要機制(69% dominant NIH);在 DES-ISR,NIH 仍佔 59%,但常與 underexpansion 共存。[2] NIH 主導的 ISR 通常在支架植入後 6–12 個月出現(BMS)或更晚期(DES)。
Neoatherosclerosis
Neoatherosclerosis 是 DES-ISR 長期失效的關鍵機制。其特徵為在既有的 neointima 內形成 lipid-laden foamy macrophages、壞死核心、甚至 plaque rupture。[1,2] OCT 研究顯示,neoatherosclerosis 在 DES-ISR 較 BMS-ISR 更頻繁且發展更快(accelerated course),這與 DES 抑制內皮化導致的 delayed healing 有關。[1] 重要的是,neoatherosclerosis 的 ISR 可以 ACS 呈現,包括 plaque rupture 與 stent thrombosis。[2]
Stent Underexpansion
Stent underexpansion 是最重要的可矯正機械性因素。在一項 IVUS 研究中,40% 的 second-generation DES-ISR 合併 stent CSA < 5 mm²。[2] Underexpansion 的原因包括:(1)初始植入時的 sizing 不足、(2)嚴重鈣化導致無法充分擴張、(3)先前未使用 IVI 引導。未矯正 underexpansion 而直接進行 DCB 或 DES 治療,是 ISR 復發的重要預測因子。[2,4]
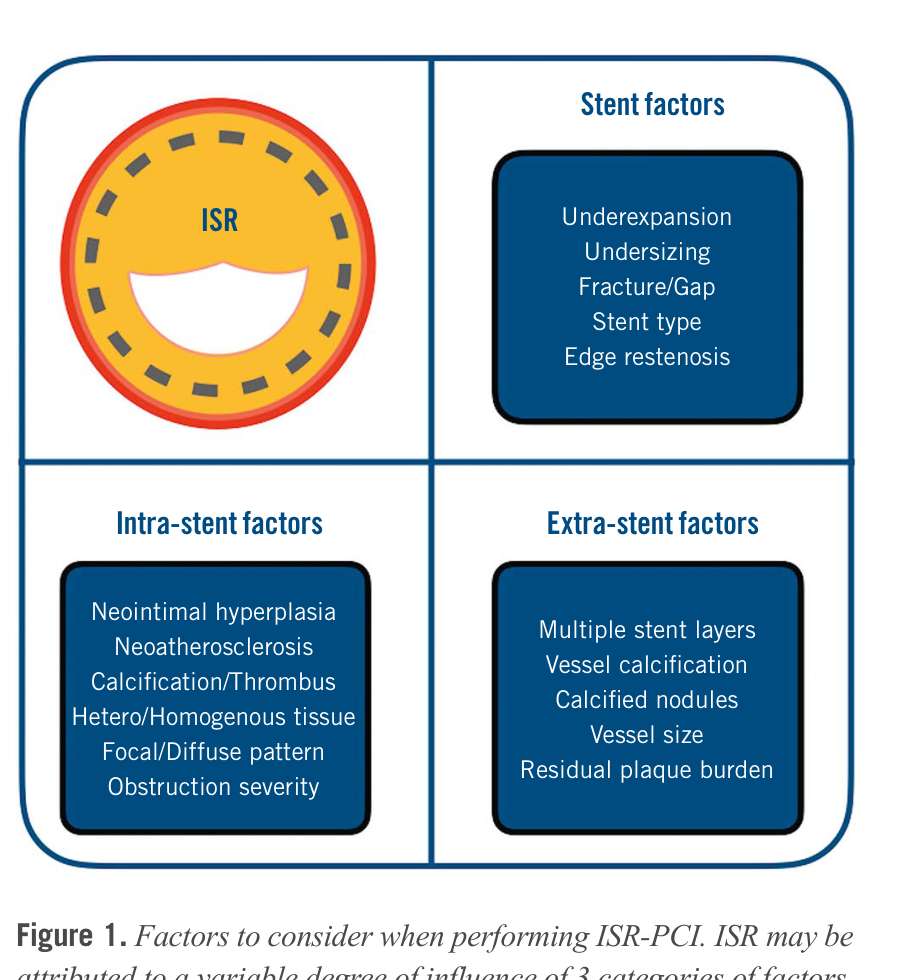
BMS-ISR vs DES-ISR:不同的疾病
| 特徵 | BMS-ISR | DES-ISR |
|---|---|---|
| 血管造影形態 | Diffuse pattern 較多 | Focal pattern 較多 |
| OCT 組織特性 | Homogeneous, high signal, most common | Layered structure 或 heterogeneous, most common |
| Late lumen loss 時程 | 6–8 個月達高峰 | 持續進行至 5 年以上 |
| 主要機制 | NIH(rich smooth muscle cells) | NIH + neoatherosclerosis(hypocellular) |
| Neoatherosclerosis | Relatively infrequent, late | Relatively frequent, accelerated |
| 治療反應 | DCB 與 DES 效果相當 | DES 較 DCB 稍優(尤其長期) |
知道原始植入的支架種類(BMS 或 DES)對治療決策非常重要。BMS-ISR 以 NIH 為主,DCB 與 DES 皆有良好效果;DES-ISR 常合併 neoatherosclerosis 與 underexpansion,DES 再植入在長期效果上稍優於 DCB。[2,5]
2B. SCAI 2023 時間分類法
2023 年 SCAI Expert Consensus 提出了新的時間導向 ISR 分類系統,補充了傳統 Mehran 形態分類的不足:[4]
| 時期 | 時間 | 主要機制 | 處理重點 |
|---|---|---|---|
| Early ISR | < 30 天 | Undersizing / underexpansion / stent fracture / recoil | IVI 評估機械問題 → 矯正 |
| Late ISR | 30 天 – 1 年 | Delayed healing / NIH / drug resistance | DCB 或 hetero-DES |
| Very Late ISR | > 1 年 | Neoatherosclerosis / NIH / stent fracture | IVI 辨別機制 → 個別化策略 |
2C. Mehran 形態分類
Mehran 分類基於血管造影形態,將 ISR 分為四型:[1]
Type I(Focal,≤10 mm): 最常見,可在支架內任何位置。治療成功率最高。
Type II(Diffuse intra-stent,>10 mm): 瀰漫性但局限在支架範圍內。
Type III(Diffuse proliferative): 超出支架邊緣。
Type IV(Total occlusion): 完全閉塞,處理最困難,常需 CTO techniques。
需注意此分類系統源自 BMS 時代,對 DES-ISR 的適用性有所限制。DES-ISR 中 focal pattern 比例較高,但形態分類無法反映底層的病理機制。[2]
2D. 風險因子
ISR 的風險因子涵蓋三個層面:[1,4]
患者因素: 糖尿病(最強獨立預測因子)、慢性腎病、左心室功能不全。
血管造影因素: 小血管(≤2.75 mm)、長病灶、分叉病灶、chronic total occlusion (CTO)。
手術因素: Stent underexpansion、geographic miss、stent fracture、multiple stent layers。
3. 診斷:影像的角色
3A. 為什麼 IVI 是必要的
ISR 的處理始於正確辨別底層機制,而單靠血管造影無法達成此目標。Intravascular imaging(IVI)——包括 optical coherence tomography(OCT)與 intravascular ultrasound(IVUS)——能提供關鍵的診斷資訊。[1,2,4]
目前各大指引均推薦使用 IVI 評估 ISR:AHA 2021 為 COR 2a[6];ESC 2024 為 Class IIa, Level B[7];SCAI 2023 Expert Consensus 則「strongly recommends routine IVI evaluation」。[4] IVI 能辨別:(1)underexpansion 與否(stent CSA < reference vessel area 的 80%)、(2)stent fracture(strut 缺失)、(3)neointimal tissue characterization(NIH vs neoatherosclerosis)、(4)edge dissection 或 geographic miss。[2,4]
目前尚無 RCT 直接證實 IVI-guided ISR treatment 改善臨床預後。推薦基於專家共識、觀察性研究、以及 de novo PCI 中 IVI 改善結果的間接證據。但臨床邏輯極為清晰:不辨別機制就治療 ISR,等同於盲目處理。[2]
3B. OCT vs IVUS
| 特徵 | OCT | IVUS |
|---|---|---|
| 解析度 | 10–20 µm(axial 12-15 µm) | ~150 µm |
| 穿透深度 | 1–2 mm(受限) | 4–8 mm(深穿透) |
| 組織特徵化 | ✅ 優異:辨別 NIH/neoatherosclerosis/thrombus | 有限:可辨別 hyperplasia/calcification |
| Stent 細節 | ✅ Strut apposition、malapposition、coverage | 可辨別 underexpansion、fracture |
| Vessel sizing | 受限(EEL 不一定看到) | ✅ 精確:EEL 清晰 |
| 多層支架 | 困難(shadowing 嚴重) | ✅ 較佳 |
| 操作需求 | 需 blood-free field(contrast flush) | 不需 blood-free field |
| ISR 最佳適應症 | Tissue characterization、neoatherosclerosis | Vessel sizing、underexpansion 評估 |
3C. OCT 組織分型
基於 OCT 表現,ISR 組織可分為四型:[2]
Homogeneous: 均勻高信號、低後散射,代表平滑肌細胞為主的 NIH。多見於 early BMS-ISR。
Heterogeneous: 混合信號強度,可能代表 proteoglycan-rich neointima 或 early neoatherosclerosis。
Attenuated: 表層高信號、深層高後散射,提示 lipid-core plaque。
Layered: 表層高信號、深層低信號,常見於 peri-strut 區域,代表進展中的 neoatherosclerosis。
OCT 上呈 homogeneous pattern 的 ISR 多為單純 NIH,DCB 或 DES 效果均佳。Heterogeneous / layered pattern 提示 neoatherosclerosis,初步數據暗示 DES 可能較 DCB 有優勢,但此假說仍需 ISAR-DESIRE 5 等前瞻性 RCT 驗證。[2]
3D. Physiologic Assessment
FFR / iFR 在 ISR 的角色有限但值得了解。先前資料顯示,血管造影中度狹窄(40-70%)的 ISR,若 FFR ≥0.75 可安全保守觀察(one-year follow-up data)。[2] 然而,目前沒有 RCT 支持以 FFR 引導 ISR 治療策略。一般建議 ISR 應遵循與 de novo CAD 相同的診斷路徑。[2]
4. 治療策略(核心章節)
Network meta-analysis 一致顯示,DES 再植入與 drug-coated balloon (DCB) 是 ISR 的兩大最佳治療策略,兩者均優於 balloon angioplasty (BA)、BMS、以及 intravascular brachytherapy (IVBT)。[1,2,5] 以下依臨床操作順序逐一討論。
4A. Lesion Preparation — 成功的關鍵前提
無論最終選擇 DCB 或 DES,充分的病灶前處理(lesion preparation)是 ISR-PCI 成功的最關鍵步驟。[2,4]
第一步:使用 non-compliant (NC) balloon 或 ultra-high-pressure non-compliant balloon (UHPNCB) 進行充分擴張,目標為殘餘狹窄 <20-30%。若遇嚴重鈣化或 underexpansion,可逐步升級至 cutting balloon、scoring balloon、甚至 atheroablation。[2,4]
「Watermelon seeding」現象:使用一般球囊擴張嚴重或 diffuse 的 ISR 時,球囊可能向兩側滑脫(geographic miss)。Cutting / scoring balloon 因其刀片或 nitinol wire 能「anchoring」在病灶上,有效減少此問題。ISAR-DESIRE 4 試驗顯示,以 scoring balloon 作為 DCB 前處理,可改善 DCB 的 anti-restenotic 效果。[2]
Alfonso 等人的治療流程建議:先以 IVI 評估 → 處理所有機械性問題(underexpansion、fracture)→ 再以 DCB 或 DES 進行最終治療 → 最後以 IVI 確認結果。[2]
4B. Drug-Coated Balloon (DCB)
DCB 由標準 angioplasty balloon 表面塗覆 antiproliferative drug(多為 paclitaxel)與 excipient matrix 組成。其核心優勢在於提供抗增生治療但不留金屬層——對多層支架 ISR 尤其有吸引力。[1,2]
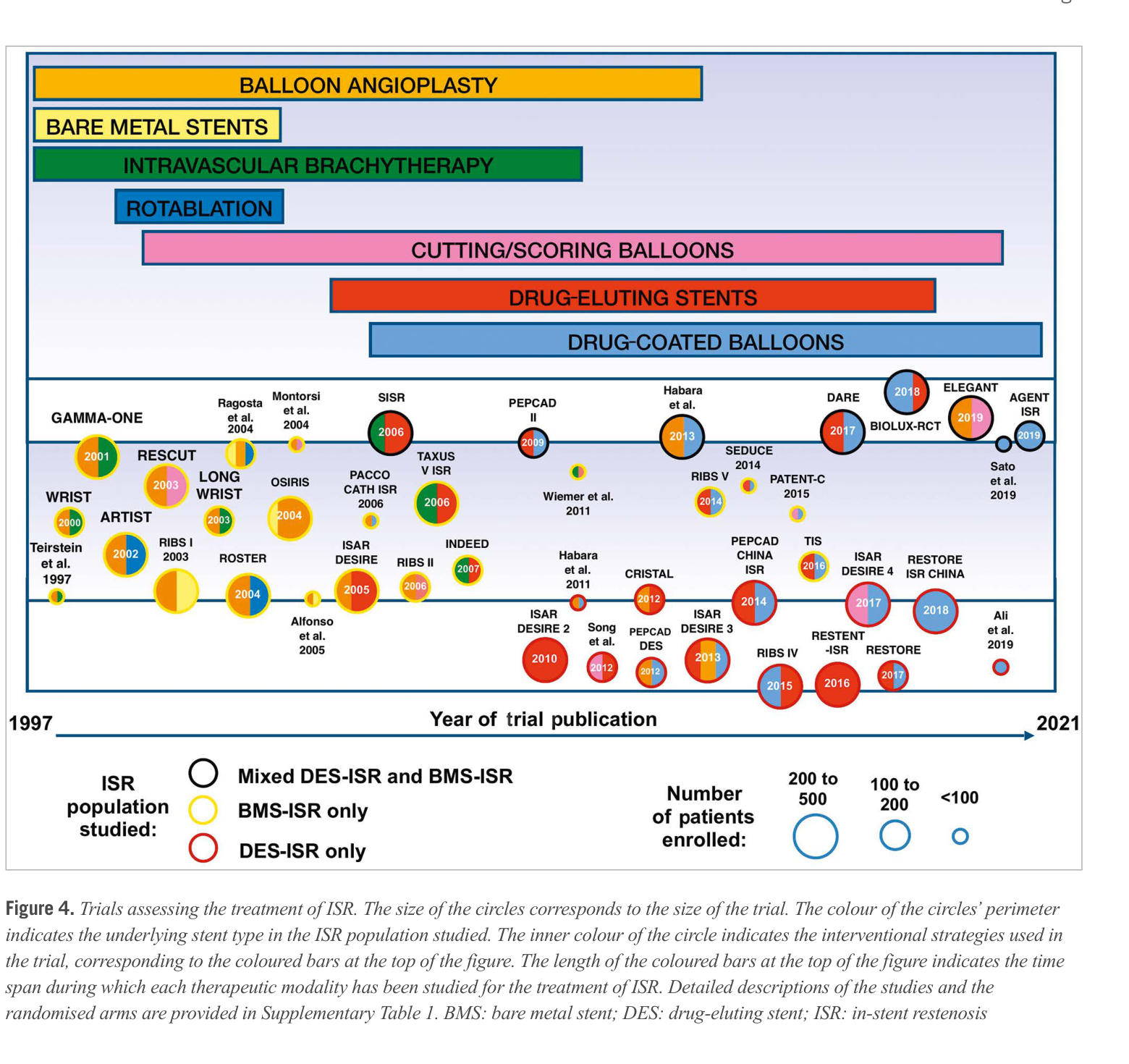
Paclitaxel DCB:核心 RCT 證據
| 試驗 | N | ISR 類型 | 比較 | 主要結果 | 結論 |
|---|---|---|---|---|---|
| DARE[8] 🔴 RCT |
278 | Any ISR (56% DES) |
DCB (SeQuent Please) vs EES (XIENCE) | 6M MLD: 1.71 vs 1.74 mm (NI met, p<0.0001) 12M MACE: 10.9% vs 9.2% (p=0.66) |
DCB 非劣於 EES |
| RIBS-IV 3yr[9] 🔴 RCT |
309 | DES-ISR only | DCB (SeQuent Please) vs EES | 3yr TLR: DCB 15.6% vs EES 7.1% (HR 0.43, p=0.015) 3yr MACE: 24.7% vs 15.5% (p=0.036) |
EES 長期較優(尤 DES-ISR) |
| AGENT IDE[10] 🔴 Landmark RCT |
600 | Any ISR (43% multi-layer) |
Agent DCB (paclitaxel, Boston Sci) vs BA | 1yr TLF: 17.9% vs 28.6% (HR 0.59, p=.003) 1yr TLR: 13.0% vs 24.7% (HR 0.50, p=.001) 1yr ST: 0 vs 3.2% (p<.001) |
DCB 顯著優於 BA → FDA approval |
| DAEDALUS[5] |
1,976 | Mixed ISR (10 RCTs) |
DES vs paclitaxel DCB | 3yr TLR: DES 10.4% vs DCB 15.1% (p=0.014) 3yr death/MI: 相當 |
DES 在 TLR 有 modest 優勢 效果受 stent type 影響 |
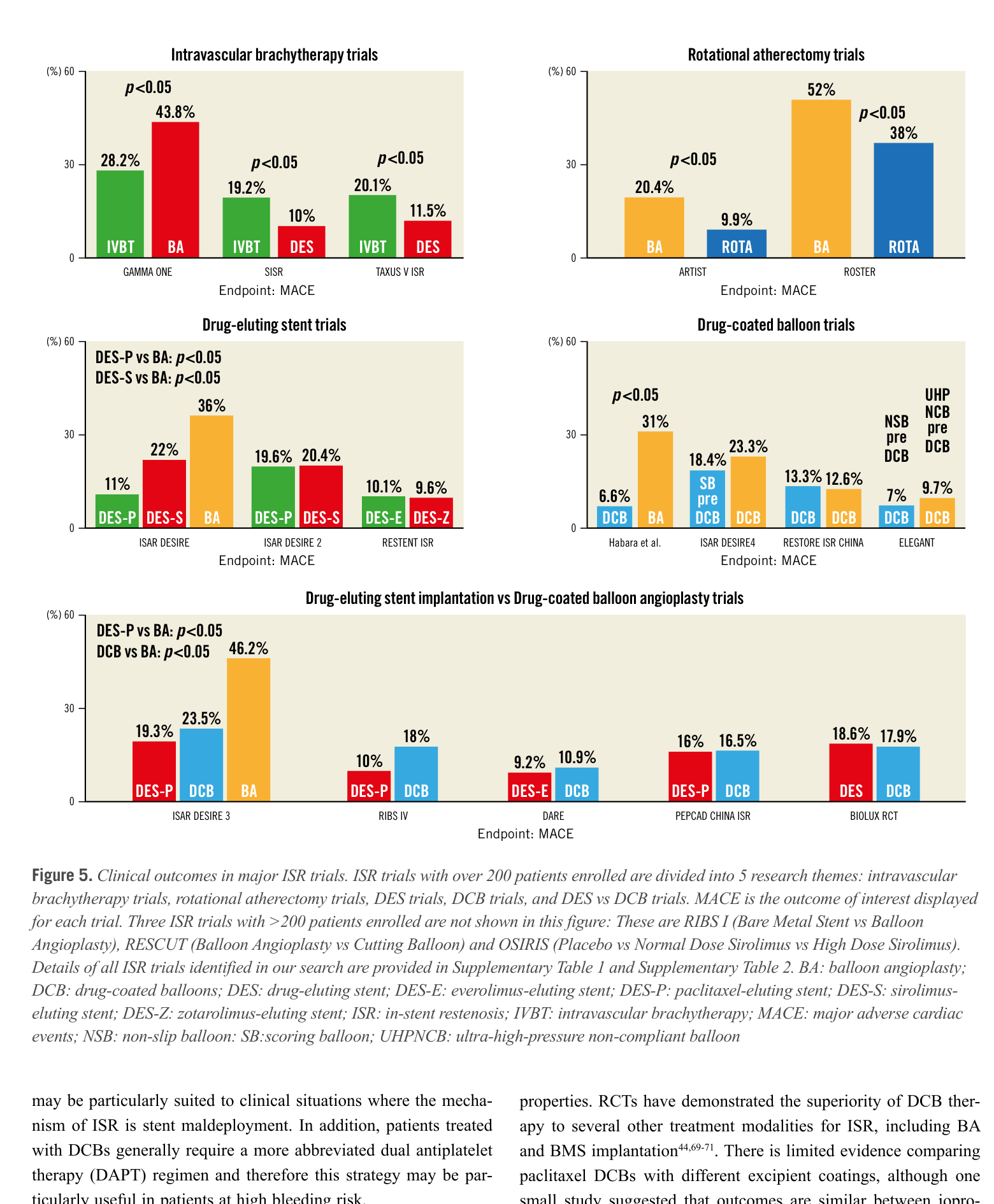
AGENT IDE Trial — 深入解析
AGENT IDE 是美國第一個核准冠狀動脈 DCB 的關鍵性 RCT(Yeh et al., JAMA 2024),也是全球最大規模的 ISR DCB 試驗。[10]
設計: 600 例 ISR 患者,40 個美國中心,2:1 隨機分配(Agent DCB 399 例 vs uncoated BA 201 例),May 2021–Aug 2022。患者族群為高風險群:51% 糖尿病、43% 多層支架 ISR、30% prior CABG、IVI 使用率 72-74%。
1 年主要結果:
| Endpoint | Agent DCB | BA Control | HR (95% CI) | P |
|---|---|---|---|---|
| TLF (primary) | 17.9% | 28.6% | 0.59 (0.42–0.84) | .003 |
| TLR | 13.0% | 24.7% | 0.50 (0.34–0.74) | .001 |
| TV-MI | 5.8% | 11.1% | 0.51 (0.28–0.92) | .02 |
| Cardiac death | 2.9% | 1.6% | 1.75 (0.49–6.28) | .38 |
| Definite/probable ST | 0% | 3.2% | — | <.001 |
多層支架亞組: 在有 ≥2 層支架的患者(n=256),TLF:Agent DCB 23.8% vs BA 40.0%(HR 0.55, 95% CI 0.34–0.87, p=.009),效益甚至更為顯著。[10]
3 年追蹤(CRT 2026 報告): TLF:DCB 32.7% vs BA 40.9%(HR 0.72, 95% CI 0.55–0.96)。Landmark analysis 顯示幾乎所有益處集中在第 1 年;1 年後兩組曲線平行。[11]
AGENT IDE 的比較對象是 uncoated BA(而非 DES),這是 FDA 法規路徑的選擇。因此,AGENT IDE 確立了 DCB 對 ISR 的 efficacy,但不能直接推論 DCB 等於或優於 DES。臨床上 DCB vs DES 的選擇仍需依據 RIBS-IV、DAEDALUS 等頭對頭試驗。[10,11]
Paclitaxel DCB 安全性
2018 年一篇 meta-analysis 引發了 paclitaxel-coated devices 在周邊血管的死亡率疑慮。Scheller 等人隨後進行了專門針對冠狀動脈 paclitaxel DCB 的大型 meta-analysis(26 RCTs, 4,590 patients):[12]
| 時間 | Endpoint | DCB vs Control RR (95% CI) | P |
|---|---|---|---|
| 1 年 | All-cause mortality | 0.74 (0.51–1.08) | .116 |
| 3 年 | All-cause mortality | 0.73 (0.53–1.00) | .047 |
| 3 年 | Cardiac mortality | 0.53 (0.33–0.85) | .009 |
| 1 年 | MI | 0.60 (0.41–0.89) | .01 |
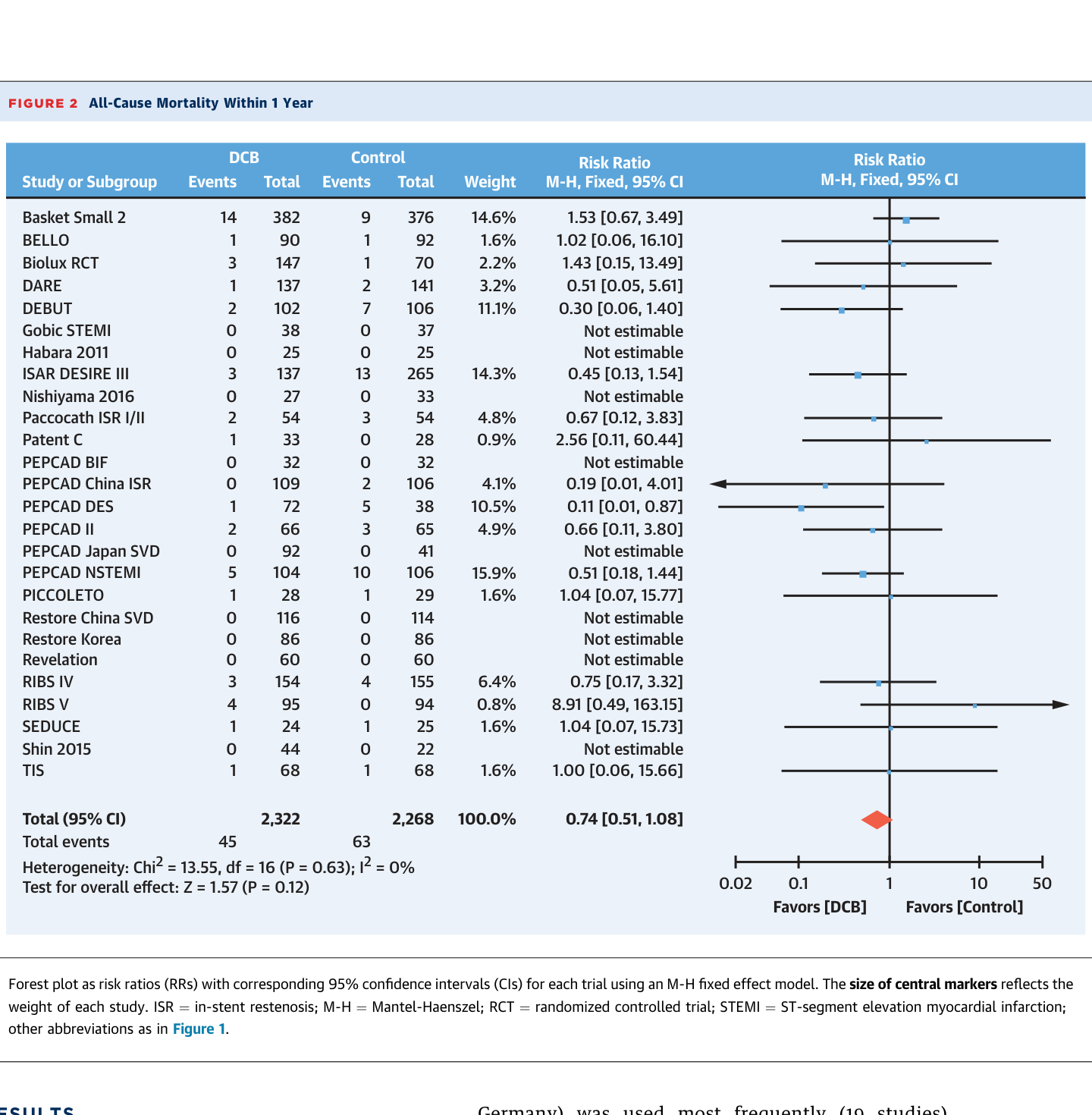
冠狀動脈 paclitaxel DCB 不增加死亡率,反而在長期(3 年)有降低 cardiac mortality 與 MI 的趨勢。周邊動脈的 paclitaxel 死亡率疑慮不適用於冠狀動脈領域。[12]
Sirolimus DCB
近年 sirolimus DCB 的開發解決了 limus 類藥物在球囊表面 binding 與 transfer 的技術挑戰。初步小型 RCT 顯示 sirolimus DCB 與 paclitaxel DCB 的 6 個月血管造影與 12 個月臨床結果相似。[2] 目前尚無大型 RCT 比較 sirolimus DCB 與 DES 或 paclitaxel DCB 在 ISR 的效果。是否存在 limus DCB 在冠狀動脈的「class effect」,仍待進一步研究。
DCB 技術要點
(1)充分預擴張至 <20% residual stenosis 是 DCB 成功的絕對前提;(2)DCB 擴張時間建議 ≥60 秒;(3)DCB 需 cover 整段病灶並在兩側各延伸 2–3 mm;(4)若出現 flow-limiting dissection → 需 bailout stenting;(5)長病灶可用兩條 DCB 做小範圍 overlap。[2,4]
4C. Drug-Eluting Stent (DES) 再植入
DES 的核心優勢在於提供最大的 acute gain(即刻管腔直徑增加),在 network meta-analysis 中始終排名第一。[1,2,5] 但其代價是增加一層金屬——在已有多層支架的患者(所謂「onion skin phenomenon」),這可能帶來更大的長期問題。[2]
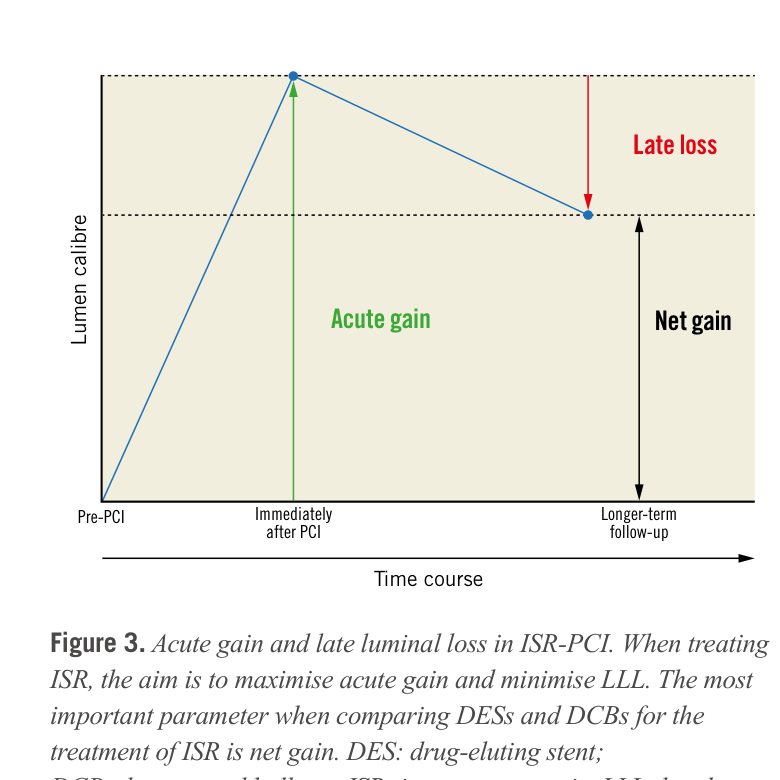
Acute Gain vs Late Lumen Loss:為什麼 Net Gain 才是關鍵
比較 DES 與 DCB 時,單看 acute gain 或 late lumen loss (LLL) 都不完整。DES 的 acute gain 顯著大於 DCB(因為有支架骨架支撐),但 DES 的 LLL 也較大。真正反映治療效果的指標是 net gain(= acute gain − LLL)。在多數頭對頭試驗中,DES 的 net gain 稍優或與 DCB 相當。[2]
DES Strategy:Hetero-DES vs Homo-DES
理論上,使用與原始支架不同藥物的 DES(hetero-DES,即「switch strategy」)可能避免藥物抗性。然而,唯一直接測試此假說的隨機試驗 ISAR-DESIRE 2 未顯示 hetero-DES 策略對 sirolimus-eluting stent ISR 有額外優勢。[2] RIBS-III 的非隨機數據暗示 hetero-DES 可能有益,但證據級別有限。目前 everolimus-eluting stent (EES) 在所有試驗中表現最佳,因此無論原始支架種類,以 EES 作為 ISR re-stenting 的首選是合理的。[1,2]
RIBS-IV 3-Year Data:DES-ISR 的關鍵長期數據
RIBS-IV 是唯一針對純 DES-ISR 族群、提供 3 年追蹤的 RCT(Alfonso et al., JACC CI 2018)。[9]
設計: 309 例 DES-ISR 患者,23 個西班牙中心,DCB (SeQuent Please, n=154) vs EES (XIENCE, n=155)。3 年臨床追蹤率 100%。
3 年結果:
| Endpoint | DCB | EES | HR (95% CI) | P |
|---|---|---|---|---|
| TLR | 15.6% | 7.1% | 0.43 (0.21–0.87) | .015 |
| TVR | 20.8% | 11.0% | 0.50 (0.28–0.90) | .017 |
| MACE (CD+MI+TLR) | 24.7% | 15.5% | — | .036 |
| Death | 5.2% | 5.8% | — | NS |
| Stent thrombosis | 2.6% | 1.3% | — | .40 |
Landmark analysis: 事件差異主要集中在第 1 年;1 年後兩組 event rate 平行。[9]
關鍵亞組: 在小血管(≤3 mm),EES 的優勢最為顯著(3yr TLR: HR 0.26, p=0.015)。[9]
RIBS-IV 的核心訊息:對 DES-ISR,EES 再植入在長期 TLR 上有 modest 但 significant 的優勢(NNT ≈12 at 3 years)。但在需要 avoid additional metal layer 的情境(多層支架、major side branch、高出血風險),DCB 仍是合理選擇。[9]
4D. DES vs DCB:如何選擇?
綜合所有 RCT、meta-analysis 與指引,以下為選擇框架:[1,2,4,5,6,7]
| 情境 | 建議首選 | 理由 |
|---|---|---|
| BMS-ISR | DCB 或 DES(comparable) | DAEDALUS subgroup: BMS-ISR 兩者效果無差異[5] |
| DES-ISR(首次) | DES(EES)稍優 | RIBS-IV: EES 3yr TLR 7.1% vs DCB 15.6%[9];ESC 2024 Class I-A[7] |
| 多層支架 ISR(≥2 layers) | DCB 優先 | 避免第 3 層金屬;AGENT IDE multilayer subgroup: HR 0.55[10] |
| 高出血風險 | DCB 優先 | DCB 後 DAPT 1–3 個月 vs DES 後 6–12 個月[2] |
| Major side branch at risk | DCB 優先 | 不留金屬 → 不 jail side branch[2] |
| Stent fracture | DES(re-stent across fracture) | 需 scaffold support[2] |
| Unknown stent type | DES(EES)稍優 | 保守策略;DES 在 NMA 中始終排名第一[1] |
4E. Network Meta-Analysis:治療排名
多項 NMA 提供了 ISR 各治療策略的排名。Giustino 等人(JACC 2022)引用的 NMA 結果顯示,以 TLR 為 endpoint 的治療效力排名為:[1]
EES > Paclitaxel DCB > Other DES > IVBT > Cutting/Scoring Balloon > BA > BMS
在 DAEDALUS(10 RCTs, 1,976 pts, individual patient data)中,DES 在 3 年 TLR 上優於 paclitaxel DCB(10.4% vs 15.1%, p=0.014),但安全性 endpoints(death, MI)完全無差異。效果差異主要存在於 DES-ISR 亞組;在 BMS-ISR 中兩者效果相當。[5]
5. 輔助治療
5A. Cutting / Scoring Balloons
Cutting balloon 使用 3-4 把微型金屬刀片(atherotome),scoring balloon 使用低 profile nitinol wire 螺旋纏繞。兩者的核心作用是:(1)在斑塊上造成 controlled incision,有利後續組織外擴(tissue extrusion);(2)「anchoring」球囊以避免 watermelon seeding。[2]
作為單獨治療,cutting/scoring balloon 無法抑制 neointimal proliferation,因此與 BA 有相似的長期限制。[2] 其最佳角色是作為 DCB 前的 lesion preparation 工具。ISAR-DESIRE 4 試驗顯示 scoring balloon 預處理可改善後續 DCB 的效果。[2] 近期亦有 drug-coated scoring balloon 的整合式設備問世,初步結果令人期待但需更多驗證。[2]
5B. Atheroablation(RA, ELCA)
Rotational atherectomy (RA): 可用於 debulk ISR 組織,但歷史 RCT(ARTIST 試驗)顯示 RA 的結果不如 BA,且手術相關併發症較多。[2] 目前 RA 在 ISR 的角色非常有限,僅在嚴重鈣化致支架無法擴張(undilatable ISR)時,作為 DCB 或 DES 治療前的輔助手段。[2,4] 「Stentablation」(以旋磨頭磨掉支架金屬)是極少數中心嘗試的 salvage 手法,有 burr entrapment 與 vessel perforation 風險,不建議常規使用。[2]
Excimer laser coronary atherectomy (ELCA): 使用紫外線波長消融組織。在 ISR 的角色主要限於嚴重鈣化的 recurrent ISR,作為 lesion preparation 的最後手段。無隨機數據支持 ELCA 在 DES-ISR 中的使用。[2]
5C. Intravascular Lithotripsy (IVL)
IVL 使用脈衝式超聲波(pulsatile shockwaves)circumferentially 修改血管鈣化。在 de novo CAD 已證實安全有效(Disrupt CAD series),ISR 中的使用為 off-label 但有越來越多的 observational evidence。[2,4]
IVL 對 ISR 的獨特價值在於處理嚴重 circumferential 鈣化導致的 undilatable stent underexpansion。與 RA 和 ELCA 相比,IVL 更為 user-friendly 且不依賴 operator experience。[2] 多份觀察性報告顯示,IVL 可成功改善先前常規方法無法擴張的 ISR。[4] 但目前無 RCT 數據。
5D. Vascular Brachytherapy (VBT)
VBT 通過在支架內輸送局部輻射(β- 或 γ-radiation)抑制 neointimal 增生。歷史 RCT(GAMMA-ONE, SISR, TAXUS V ISR)顯示 VBT 優於 BA,但在 DES 問世後已被迅速取代。[2] 目前 VBT 的角色僅限於 recurrent ISR 的最後手段。AHA 2021 給予 COR 2b(may be considered for recurrent ISR)。[6] 大多數中心已無 VBT 設備。
5E. CABG — Heart Team 決策
CABG 在以下 ISR 情境中應被考慮:[2,4,6]
(1)反覆 PCI 失敗的 diffuse recurrent ISR;(2)Left main stem ISR(尤其合併多血管病變);(3)Ostial LAD ISR 合併 multivessel disease;(4)ISR 合併 significant LV dysfunction。
AHA 2021 建議:symptomatic recurrent diffuse ISR → COR 2a,考慮 CABG(Heart Team decision)。[6] SCAI 2023 Consensus 也明確列出 CABG 的適應症表格。[4] 值得注意的是,ISR 患者接受 CABG 的 operative risk 通常高於 de novo CAD(先前多次 PCI 的血管解剖複雜性),需個別評估。
6. DAPT:ISR-PCI 後的抗血小板策略
目前沒有專門針對 ISR-PCI 後 DAPT duration 的 RCT,臨床決策參考 de novo PCI 的數據外推。[2]
DCB 後
DCB 不留金屬,理論上內皮化需求較低,DAPT 可較短。多數試驗使用的 protocol 為 DAPT 1–3 個月(aspirin + P2Y₁₂ inhibitor),之後轉為 aspirin 單藥。對高出血風險患者,DCB 的 shorter DAPT 是其重要臨床優勢。[2,4]
DES 後
ISR-PCI with DES 的 DAPT 通常遵循 de novo PCI 建議:6–12 個月,視臨床情境(ACS vs CCS、bleeding risk)調整。[6,7]
延長 DAPT 的考量
PRODIGY 試驗的 subanalysis 顯示,ISR-PCI 後使用 24 個月延長 DAPT(相較 6 個月)可能有益。[2] 然而,此為事後亞組分析,證據等級有限。一般原則:DAPT 的 composition(P2Y₁₂ inhibitor 選擇)與 duration 應依患者的缺血風險與出血風險做個別化決定。
ISR 患者「高出血風險 + 多層支架」的組合很常見。此時 DCB 可一舉解決兩個問題:不增加金屬層 + 允許 shorter DAPT。這是 DCB 在真實世界臨床中被廣泛採用的重要原因。[2,4]
7. 指引推薦總整理
| 主題 | AHA 2021[6] | ESC 2024[7] | SCAI 2023[4] |
|---|---|---|---|
| IVI 用於 ISR 評估 | COR 2a | Class IIa, Level B (encouraged) |
Strongly recommended (routine) |
| DES 治療 ISR | COR 1, LOE A | Class I, Level A (DES recommended over DCB for DES-ISR) |
Recommended (especially for DES-ISR) |
| DCB 治療 ISR | COR 1, LOE A (與 DES 並列) |
Class I, Level A (但 DES-ISR 時 DES 優先) |
Recommended (especially for BMS-ISR & multi-layer) |
| CABG | COR 2a (recurrent diffuse ISR) |
未單獨列出 ISR CABG 推薦 | 考慮於 LMS-ISR, recurrent ISR, multivessel |
| VBT | COR 2b (recurrent ISR) |
未提及 | 最後手段,大多數中心已棄用 |
| Lesion Preparation | 未具體推薦 | Ultra-high-pressure balloon, cutting/scoring balloon, IVL, RA for lesion preparation |
Strongly emphasized as essential first step |
ESC 2024 與 AHA 2021 的最大差異在於:ESC 2024 明確推薦 DES-ISR 時 DES 優於 DCB(Class I, Level A),而 AHA 2021 將兩者並列。[6,7] 這反映了 RIBS-IV 3-year 與 DAEDALUS meta-analysis 在 2022 年後被納入證據基礎的結果。SCAI 2023 Consensus 則更強調 IVI 的角色與 lesion preparation 的重要性。[4]
8. 特殊情境
8A. Recurrent ISR / Multi-Layer ISR
Recurrent ISR(ISR 治療後再次 ISR)是最具挑戰性的情境之一。在 RIBS 系列研究中,ISR 經 DES 再植入後可能出現第 3 層、甚至第 4 層支架。一項研究顯示,3 層支架的 1-year TLR 高達 41.2%(相較於 1 層 14.5% 和 2 層 14.9%)。[2]
處理原則:(1)回頭檢視先前 ISR 治療的 IVI 影像:是否有未解決的 mechanical issues(persistent underexpansion);(2)若有 mechanical issues → 必須先解決(IVL, RA, ELCA as needed);(3)避免第 3 層金屬 → DCB 為首選;(4)若 DCB 也失敗 → 考慮 VBT 或 CABG(Heart Team)。[2,4]
AGENT IDE 的多層支架亞組數據(TLF HR 0.55)強化了 DCB 在此情境的角色。[10] 此外,一項 meta-analysis 顯示 VBT 在 recurrent ISR 中,2 年 TVR 約 25%(1/4 patients),效果仍不理想。[2]
8B. Left Main Stem ISR
Left main stem (LMS) ISR 的數據有限。FAILS study(718 例 LMS stent 失效)顯示大多數可以 PCI 處理。[2] 回顧性分析顯示 DES 與 DCB 在 LMS-ISR 效果相當。但LMS stent failure 後的死亡率不低——這使得 CABG 在合適患者中成為重要選項。[2]
8C. ISR-CTO
ISR-CTO 在 Mehran 分類中屬 Type IV,佔 ISR 的一小部分但處理難度最高。ISR-CTO PCI 的成功率與併發症率因報告不同而差異很大。[2] 術中支架的可視化(不同角度投影)可為 CTO 導線操作提供路徑圖(roadmap)。ISR-CTO PCI 應被視為高度專業化、高風險的手術,建議在有 CTO 經驗的中心進行。[2]
8D. Stent Fracture
Stent fracture 在血管造影上表現為支架 strut 的完全或不完全分離,可由 IVUS 上 strut 缺失(at least 1 slice)辨別。[2] Fracture 導致的 ISR 在大多數情況下需要 re-stenting(覆蓋 fracture segment)。雖然直覺上 DES 是 fracture-ISR 的首選(需要 scaffold support),但目前沒有高品質隨機數據。[2]
9. 臨床決策流程圖


以下流程圖整合自 Alfonso et al.(EuroIntervention 2022)與 SCAI 2023 Consensus 的建議:[2,4]
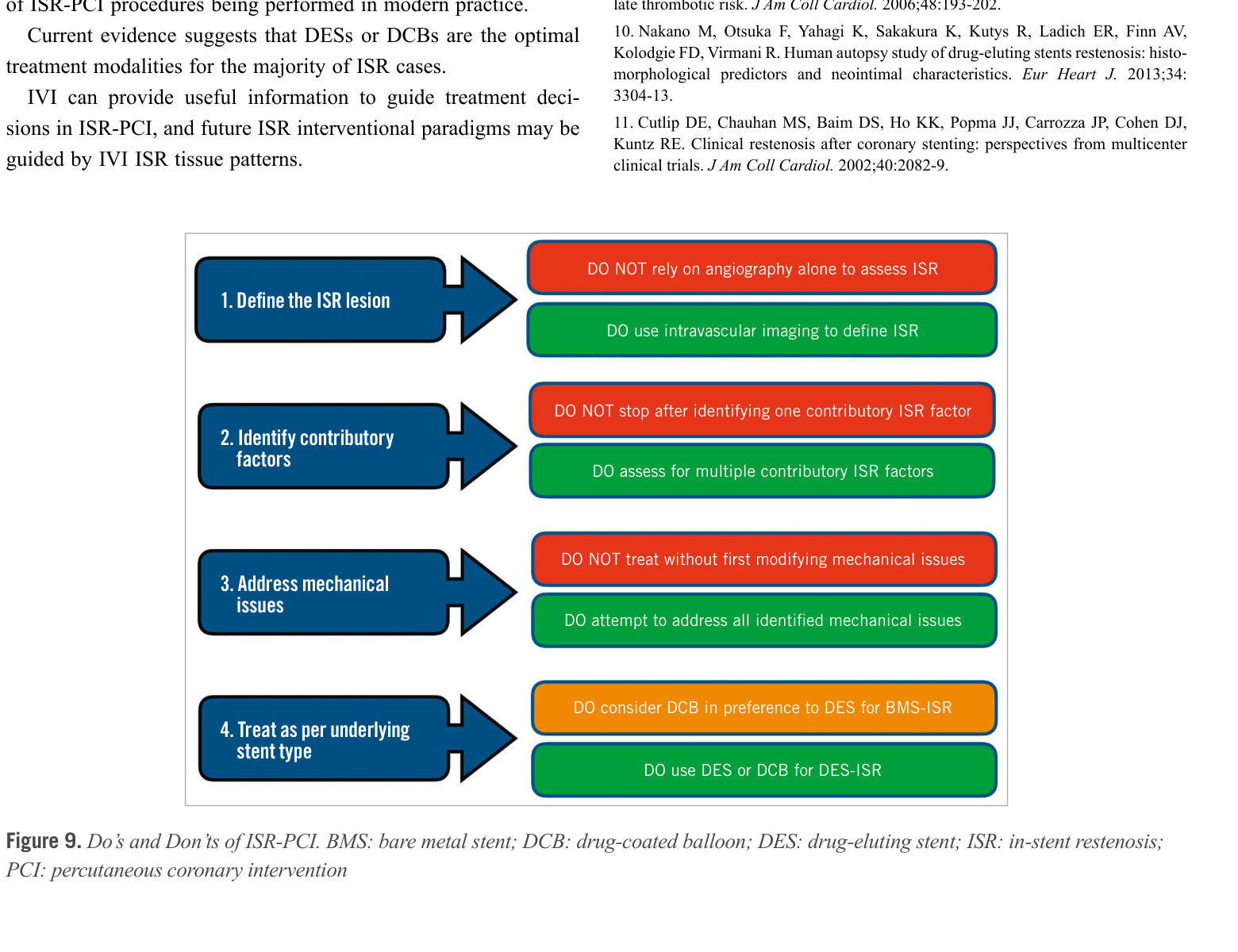
Alfonso et al. 同時提出了 ISR-PCI 的「Do's and Don'ts」:[2]
| ✅ DO | ❌ DON'T |
|---|---|
| DO use intravascular imaging to define ISR | DON'T rely on angiography alone to assess ISR |
| DO assess for multiple contributory ISR factors | DON'T stop after identifying one contributory ISR factor |
| DO attempt to address all identified mechanical issues | DON'T treat without first modifying mechanical issues |
| DO consider DCB in preference to DES for BMS-ISR | DON'T use DCB if residual stenosis >30% after preparation |
| DO use DES or DCB for DES-ISR | DON'T add a 3rd stent layer if avoidable |
參考文獻
- Giustino G, Colombo A, Camaj A, et al. Coronary In-Stent Restenosis: JACC State-of-the-Art Review. J Am Coll Cardiol. 2022;80(4):348-372. PMID: 35863852. 🟢 Review
- Alfonso F, Coughlan JJ, Giacoppo D, Kastrati A, Byrne RA. Management of in-stent restenosis. EuroIntervention. 2022;18:e103-e123. PMID: 35656726. DOI: 10.4244/EIJ-D-21-01034. 🟢 State-of-Art Review
- Moussa ID, Mohananey D, Saucedo J, et al. Trends and Outcomes of Restenosis After Coronary Stent Implantation in the United States. J Am Coll Cardiol. 2020;76:1521-31. PMID: 32943166.
- Klein AJ, Amoroso NS, Engstrøm T, et al. SCAI Expert Consensus Statement on the Management of In-Stent Restenosis and Stent Thrombosis. JSCAI. 2023;2(4):100971. PMID: 39131655. 🔵 Consensus
- Giacoppo D, Alfonso F, Xu B, et al. Paclitaxel-coated balloon angioplasty vs. drug-eluting stenting for the treatment of coronary in-stent restenosis: a comprehensive, collaborative, individual patient data meta-analysis of 10 randomized clinical trials (DAEDALUS). Eur Heart J. 2020;41:3715-28. PMID: 31511862.
- Lawton JS, Tamis-Holland JE, Bangalore S, et al. 2021 ACC/AHA/SCAI Guideline for Coronary Artery Revascularization. J Am Coll Cardiol. 2022;79:e21-e129. PMID: 34882436. 🔵 Guideline
- Vrints C, Andreotti F, Koskinas KC, et al. 2024 ESC Guidelines for the management of chronic coronary syndromes. Eur Heart J. 2024;45:3415-3537. PMID: 39210710. 🔵 Guideline
- Baan J Jr, Claessen DGAJ, Lambrecht HJ, et al. A randomized comparison of paclitaxel-eluting balloon versus everolimus-eluting stent for the treatment of any in-stent restenosis: the DARE trial. JACC Cardiovasc Interv. 2018;11:275-283. PMID: 29413242. 🔴 RCT
- Alfonso F, Pérez-Vizcayno MJ, Cárdenas A, et al. A Prospective Randomized Trial of Drug-Eluting Balloons Versus Everolimus-Eluting Stents in Patients With In-Stent Restenosis of Drug-Eluting Stents: The RIBS IV Randomized Clinical Trial. J Am Coll Cardiol. 2015;66:23-33. PMID: 26139054; 3-year data: JACC Cardiovasc Interv. 2018;11:981-991. PMID: 29798776. 🔴 RCT
- Yeh RW, Bachinsky W, Engstrøm T, et al. Effect of a Paclitaxel-Coated Balloon vs an Uncoated Balloon for In-Stent Restenosis: The AGENT IDE Randomized Clinical Trial. JAMA. 2024;331(13):1119-1129. PMID: 38460161. DOI: 10.1001/jama.2024.1361. 🔴 Landmark RCT
- Yeh RW. AGENT IDE 3-Year Results. Presented at CRT 2026, Washington DC, March 2026. (Source: TCTMD, 2026-03-11). 🟢 Conference Report
- Scheller B, Vukadinovic D, Engstrøm T, et al. Survival After Coronary Revascularization With Paclitaxel-Coated Balloons. J Am Coll Cardiol. 2020;75:1017-28. PMID: 32138961.
- Mehran R, Dangas G, Abizaid AS, et al. Angiographic patterns of in-stent restenosis: classification and implications for long-term outcome. Circulation. 1999;100:1872-8. PMID: 10545431.
- Kastrati A, Mehilli J, von Beckerath N, et al; ISAR-DESIRE Study Investigators. Sirolimus-eluting stent or paclitaxel-eluting stent vs balloon angioplasty for prevention of recurrences in patients with coronary in-stent restenosis: a randomized controlled trial. JAMA. 2005;293:165-71. PMID: 15632335. 🔴 RCT
- Alfonso F, Pérez-Vizcayno MJ, García Del Blanco B, et al; RIBS V Investigators. Drug-Coated Balloon Angioplasty Versus Drug-Eluting Stent Implantation in Patients With Coronary Stent Restenosis. J Am Coll Cardiol. 2020;78:2664-78. PMID: 31492486.
- Alfonso F et al. RIBS IV + V + VI pooled analysis: 3-year outcomes. Presented at EuroPCR 2024; concurrently published in JACC Cardiovasc Interv. 2024. (Source: TCTMD). 🟢 Conference Report
本文件為教學用途綜述,基於 2018–2026 年公開文獻整理。
所有數據均引自原始文獻,未進行自行推論或延伸。
臨床決策應依個別患者狀況,由治療團隊綜合判斷。
Generated 2026-03-15 | 憤怒鳥 🐦🔥 Medical Literature Review System